题目内容
13.在如图所示的串联装置中,发现灯泡不亮,但若向其中一个烧杯中加水,则灯泡会亮起来:则:
(1)加水的烧杯为C
(2)若各烧杯中溶质的物质的量浓度相等,则A、D两烧杯中溶液导电能力最强(填“A”“B““C“或“D”)
(3)写出D烧杯中电解质的电离方程式:Ba(OH)2═Ba2++2OH-.
分析 (1)酸在水溶液中才导电;
(2)溶液导电能力与离子浓度成正比,同物质的量浓度的下列溶液导电能力最强,说明该溶液中离子浓度最大,据此分析解答;
(3)氢氧化钡时强电解质,能完全电离出钡离子和氢氧根离子.
解答 解:(1)磷酸在水溶液中才导电,作电解质,所以加水的烧杯为C,故答案为:C;
(2)质的物质的量浓度相等的硫酸和氢氧化钡溶液的离子浓度大于硫酸铜溶液的浓度,而磷酸是弱电解质,离子浓度最小,导电能力最弱,所以A、D两烧杯中溶液导电能力最强,故答案为:A、D;
(3)氢氧化钡时强电解质,能完全电离出钡离子和氢氧根离子,即Ba(OH)2═Ba2++2OH-,故答案为:Ba(OH)2═Ba2++2OH-.
点评 本题考查学生电解质的电离以及原电池的工作原理知识,属于综合知识的考查,难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8.氢镍电池是近年开发出来的可充电电池,它可以取代会产生污染的铜镍电池.氢镍电池的总反应式是:$\frac{1}{2}{H_2}+NiOOH$$?_{放电}^{充电}$Ni(OH)2据此反应式判断,下列叙述中不正确的是( )
| A. | 电池放电时,电池负极周围溶液的PH不断增大 | |
| B. | 电池放电时,正极的电极反应为:NiOOH+e-+H2O=Ni(OH)2+OH- | |
| C. | 电池充电时,阳极周围溶液的PH不断减小 | |
| D. | 电池充电时,阴极的电极反应为:2H2O+2e-=H2+2OH- |
9.人生病时要合理用药.下列药品与其作用不相匹配的是( )
| A. | 青霉素--抗菌消炎 | B. | 阿司匹林--抗过敏 | ||
| C. | 碘酒--伤口消炎 | D. | 胃舒平--抑酸止胃痛 |
1.下列实验室制气体的措施或方法中主要利用的是原电池反应原理的是( )
| A. | 实验室制H2时,向Zn和稀硫酸反应体系中加入少量的CuSO4固体 | |
| B. | 实验室制O2时,向H2O2溶液中加入少量的MnO2 | |
| C. | 实验室制CO2时,用盐酸和CaCO3反应 | |
| D. | 实验室制NH3时,加热Ca(OH)2和NH4Cl和混合物 |
8.NaCl是一种化工原料,可以制备一系列物质(见图).下列说法正确的是( )


| A. | 常温下干燥的Cl2能用钢瓶贮运,所以Cl2不与铁反应 | |
| B. | 石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂 | |
| C. | 25℃,NaHCO3在水中的溶解度比Na2CO3的大 | |
| D. | 图中所示转化反应都是氧化还原反应 |
18.下列有关化学用语正确的是( )
| A. | NH4Cl的电子式: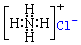 | B. | 中子数为18的氯原子:${\;}_{17}^{35}$Cl | ||
| C. | 碳酸的电离:H2CO3?2H++CO32- | D. | 次氯酸的结构式:H-Cl-O |
5.分离下列混合物,按溶解、过滤、蒸发的操作顺序进行的是( )
| A. | 硝酸钠、氢氧化钠 | B. | 氧化铜、二氧化锰 | C. | 二氧化锰、氯化钾 | D. | 硫酸铜、氢氧化钙 |