题目内容
 A、B、C、D、E五种物质都含同一种元素,C为一种淡黄色的固体.它们按如图所示的关系相互转化,已知A为单质.分别写出有关反应的化学方程式.
A、B、C、D、E五种物质都含同一种元素,C为一种淡黄色的固体.它们按如图所示的关系相互转化,已知A为单质.分别写出有关反应的化学方程式.(1)用化学式来表示下列物质:B:
(2)写出以下几步反应的化学方程式
A→C:
C→E:
(3)固体F中有杂质E,请写出所加的试剂和操作是
考点:无机物的推断,钠的重要化合物
专题:推断题,几种重要的金属及其化合物
分析:C为一种淡黄色的固体,转化关系知识利用单质A在空气中点燃反应生成推断则C为Na2O2,A为Na,D为NaOH,B为Na2O,E为碳酸钠,F为NaHCO3,以此来解答.
解答:
解:图表转化关系分析判断,C为一种淡黄色的固体,转化关系知识利用单质A在空气中点燃反应生成,推断则C为Na2O2,A为Na,D为NaOH,B为Na2O,E为碳酸钠,F为NaHCO3;
(1)上述分析判断BDE的化学式为:B为Na2O,D为NaOH,E为Na2CO3;
故答案为:Na2O,NaOH,Na2CO3;
(2)A→C的反应是钠点燃反应生成过氧化钠的反应,化学方程式为:2Na+O2
Na2O2,反应中氧气是氧化剂;
C→E的反应是过氧化钠和二氧化碳反应生成碳酸钠和氧气,反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2 ,反应中氧化产物是元素化合价升高失电子被氧化得到的产物,依据化学方程式元素化合价变化可知氧化产物为O2;
故答案为:2Na+O2
Na2O2,O2;2Na2O2+2CO2=2Na2CO3+O2 ,O2 ;
(3)固体F中有杂质E,F为NaHCO3,E为Na2CO3,固体加入蒸馏水溶解后通入足量二氧化碳气体得到碳酸氢钠溶液,低压蒸干得到碳酸氢钠固体,反应的化学方程式为:Na2CO3+CO2+H2O=2NaHCO3;
故答案为:固体加入蒸馏水溶解后通入足量二氧化碳气体得到碳酸氢钠溶液,低压蒸干得到碳酸氢钠固体,Na2CO3+CO2+H2O=2NaHCO3;
(1)上述分析判断BDE的化学式为:B为Na2O,D为NaOH,E为Na2CO3;
故答案为:Na2O,NaOH,Na2CO3;
(2)A→C的反应是钠点燃反应生成过氧化钠的反应,化学方程式为:2Na+O2
| ||
C→E的反应是过氧化钠和二氧化碳反应生成碳酸钠和氧气,反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2 ,反应中氧化产物是元素化合价升高失电子被氧化得到的产物,依据化学方程式元素化合价变化可知氧化产物为O2;
故答案为:2Na+O2
| ||
(3)固体F中有杂质E,F为NaHCO3,E为Na2CO3,固体加入蒸馏水溶解后通入足量二氧化碳气体得到碳酸氢钠溶液,低压蒸干得到碳酸氢钠固体,反应的化学方程式为:Na2CO3+CO2+H2O=2NaHCO3;
故答案为:固体加入蒸馏水溶解后通入足量二氧化碳气体得到碳酸氢钠溶液,低压蒸干得到碳酸氢钠固体,Na2CO3+CO2+H2O=2NaHCO3;
点评:本题考查无机物的推断,C为解答本题的突破口,注意常见的淡黄色固体,侧重钠及其化合物的转化的考查,明确反应即可解答,注意除杂实验设计,题目难度不大.

练习册系列答案
相关题目
配制100mL 1.00mol/L NaCl 溶液,下列说法正确的是( )
| A、将所需量的NaCl溶于100mL水中 |
| B、将所需量的NaCl溶于少量水中,再加水定容到100mL |
| C、将所需量的NaCl直接放入容量瓶中,加水定容到100mL |
| D、定容时俯视读刻度 |
在卤代烃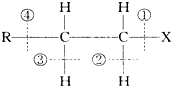 中化学键的叙述中,下列说法不正确的是( )
中化学键的叙述中,下列说法不正确的是( )
 中化学键的叙述中,下列说法不正确的是( )
中化学键的叙述中,下列说法不正确的是( )| A、当该卤代烃发生取代反应时,被破坏的键是①和② |
| B、当该卤代烃发生消去反应时,被破坏的键是①和③ |
| C、当该卤代烃在碱性条件下发生水解反应时被破坏的键是① |
| D、当该卤代烃发生消去反应时,被破坏的键是①和④ |
下列各组物质的性质及粒子变化正确的是( )
| A、酸性HClO4>H2SO4>H3PO4>H2CO3 |
| B、稳定性H2S>HCl>HBr>HI |
| C、粒子半径Br->K+>S2->S |
| D、还原性Na>Br->Cl->S2- |
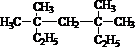 系统命名为
系统命名为 (1)已知:CH3COOH为弱电解质,在醋酸溶液中,当改变条件后,完成表格中的变化情况
(1)已知:CH3COOH为弱电解质,在醋酸溶液中,当改变条件后,完成表格中的变化情况