题目内容
10.化学与生产、生活密切相关,下列事实的解释正确的是 ( )| 选项 | 事实 | 解释 |
| A | 酸雨的pH<5.6 | CO2溶解在雨水中 |
| B | 稻草、甘蔗渣可用来造纸 | 稻草、甘蔗渣富含纤维素 |
| C | 化石燃料燃烧时采取固硫措施 | 提高化石燃料的利用率 |
| D | 将水中的铁闸门连接电源的负极而防腐 | 利用牺牲阳极的阴极保护法 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.CO2溶解在雨水中,如达到饱和,pH=5.6;
B.稻草、甘蔗渣富含纤维素,可用于造纸;
C.化石燃料燃烧时采取固硫措施,可减少二氧化硫的污染;
D..将水中的铁闸门连接电源的负极而防腐,为外加电源的阴极保护法.
解答 解:A.酸雨的pH<5.6,是由于溶液二氧化硫、氮氧化物的原因,而CO2溶解在雨水中,如达到饱和,pH=5.6,故A错误;
B.纸张的主要成分为纤维素,稻草、甘蔗渣富含纤维素,可用于造纸,故B正确;
C.化石燃料燃烧时采取固硫措施,可减少二氧化硫的污染,与提高效率无关,故C错误;
D..将水中的铁闸门连接电源的负极而防腐,为外加电源的阴极保护法,故D错误.
故选B.
点评 本题考查物质的性质及应用,为高频考点,把握物质的组成、性质为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.Q、W、X、Y、Z是原子序数依次增大的短周期元素,Q和Y均满足主族序数与周期序数相等,Q与X、W与Z同主族,Q和W能形成原子个数之比为1:1和2:1的常见化合物.下列说法正确的是( )
| A. | 原子半径:Z>Y>X>W>Q | |
| B. | Q、X形成的化合物的电子式为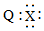 | |
| C. | 最简单氢化物的稳定性:Z>W | |
| D. | 工业上常用电解的方法制备X、Y的单质 |
9.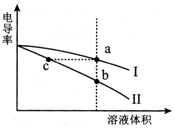 电导率是衡量电解质溶液导电能力大小的物理量.常温下,将相同体积的氢氧化钠溶液和醋酸溶液分别加水稀释,溶液的电导率随溶液体积变化的曲线如图所示.下列说法正确的是( )
电导率是衡量电解质溶液导电能力大小的物理量.常温下,将相同体积的氢氧化钠溶液和醋酸溶液分别加水稀释,溶液的电导率随溶液体积变化的曲线如图所示.下列说法正确的是( )
 电导率是衡量电解质溶液导电能力大小的物理量.常温下,将相同体积的氢氧化钠溶液和醋酸溶液分别加水稀释,溶液的电导率随溶液体积变化的曲线如图所示.下列说法正确的是( )
电导率是衡量电解质溶液导电能力大小的物理量.常温下,将相同体积的氢氧化钠溶液和醋酸溶液分别加水稀释,溶液的电导率随溶液体积变化的曲线如图所示.下列说法正确的是( )| A. | I表示NaOH溶液加水稀释过程中溶液电导率的变化 | |
| B. | a、b、c三点溶液的pH:b>c>a | |
| C. | 将a、b两点溶液混合,所得溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | |
| D. | a点水电离出的n(H+)等于c点水电离出的n(H+) |
15.已知X、Y、Z、W为短周期主族元素,在周期表中的相对位置如图,有下列说法:
①若HmXOn为强酸,则X的氢化物溶于水一定显酸性(m、n均为正整数)
②若四种元素均为金属,则Z的最高价氧化物对应的水化物一定为强碱
③若四种元素均为非金属,则W的最高价氧化物对应的水化物一定为强酸
④若四种元素只有一定为金属,则Z与Y的最高价氧化物对应的水化物一定为强酸.
其中不正确的说法有几项( )
①若HmXOn为强酸,则X的氢化物溶于水一定显酸性(m、n均为正整数)
②若四种元素均为金属,则Z的最高价氧化物对应的水化物一定为强碱
③若四种元素均为非金属,则W的最高价氧化物对应的水化物一定为强酸
④若四种元素只有一定为金属,则Z与Y的最高价氧化物对应的水化物一定为强酸.
其中不正确的说法有几项( )
| X | Y |
| Z | W |
| A. | 1项 | B. | 2项 | C. | 3项 | D. | 4项 |
2.下列化合物不能由单质之间直接化合得到的是( )
| A. | FeS | B. | SO3 | C. | FeCl3 | D. | NH3 |
19.下列除杂方案中,括号内为除去杂质所需的药品,其中正确的是( )
| A. | NaOH溶液中混有Ba(OH)2(CuSO4) | B. | Cu(NO3)2溶液中混有AgNO3(铜粉) | ||
| C. | CO2中混有CO(炽热的炭) | D. | CO2中混有HCl气体(NaOH溶液) |
20.以下电离方程式错误的是( )
| A. | MgCl2═Mg2++2Cl- | B. | Fe2(SO4)3═2Fe3++3SO42- | ||
| C. | NaHCO3═Na++H++CO32- | D. | KHSO4═K++H++SO42- |