题目内容
3.下列溶液中粒子的物质的量浓度关系正确的是( )| A. | 0.1 mol/L NaHCO3溶液与0.1 mol/L NaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-) | |
| B. | 20 mL 0.1 mol/L CH3COONa溶液与10 mL 0.1 mol/L HCl溶液混合后溶液呈酸性,所得溶液中:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+) | |
| C. | 室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)+c(H+)>c(NH4+)+c(OH-) | |
| D. | 0.1 mol/L CH3COOH溶液与0.1 mol/L NaOH溶液等体积混合,所得溶液中:c(OH-)>c(H+)+c(CH3COOH) |
分析 A、0.1 mol/L NaHCO3溶液与0.1 mol/L NaOH溶液等体积混合,生成碳酸钠溶液,碳酸根水解使溶液呈碱性;
B、20 mL 0.1 mol/L CH3COONa溶液与10 mL 0.1 mol/L HCl溶液混合后生成等物质的量的CH3COONa、NaCl、CH3COOH,溶液呈酸性,说明醋酸的电离大于醋酸根的水解;
C、pH=12的氨水与pH=2的盐酸中,氨水浓度大于盐酸,等体积混合,氨水过量,溶液呈碱性;
D、0.1mol•L-1CH3COOH溶液与0.1mol•L-1Na0H溶液等体积混合,恰好生成醋酸钠,水解显碱性.
解答 解:A、0.1 mol/L NaHCO3溶液与0.1 mol/L NaOH溶液等体积混合,生成碳酸钠溶液,碳酸根水解成碱性,离子浓度大小为c(Na+)>c(CO32-)>c(OH-)>c(HCO3-),故A错误;
B、20 mL 0.1 mol/L CH3COONa溶液与10 mL 0.1 mol/L HCl溶液混合后生成等物质的量的CH3COONa、NaCl、CH3COOH,溶液呈酸性,说明醋酸的电离大于醋酸根的水解,故c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+),故B正确;
C、pH=12的氨水与pH=2的盐酸中,氨水浓度大于盐酸,等体积混合,氨水过量,溶液呈碱性,所以c(OH-)>c(H+),溶液中存在电荷守恒c(NH4+)+c(H+)=c(Cl-)+c(OH-),所以得c(NH4+)>c(Cl-),c(Cl-)+c(H+)<c(NH4+)+c(OH-),故C错误;
D、0.1mol•L-1CH3COOH溶液与0.1mol•L-1Na0H溶液等体积混合,恰好生成醋酸钠,醋酸根离子水解,根据质子守恒可知c(OH-)=c(H+)+c(CH3COOH),故D错误;
故选B.
点评 本题考查酸碱混合溶液的定性分析及离子浓度大小的比较,把握混合后溶液中的溶质及盐类水解规律、电荷守恒等为解答的关键,题目难度不大.

 快乐5加2金卷系列答案
快乐5加2金卷系列答案| A. | Y的氢化物的沸点比R的氢化物的沸点高 | |
| B. | Z、W、R按最高价氧化物对应水化物的酸性强弱排列顺序是R>W>Z | |
| C. | X2Y2化合物中的化学键与X2R中的化学键类型完全相同 | |
| D. | RY2通入Ba(NO3)2溶液中有白色沉淀生成,该沉淀不溶于硝酸 |
| 溶质 | NaF | NaClO | Na2CO3 |
| pH | 7.5 | 9.7 | 11.6 |
| A. | 根据上表,向足量NaClO溶液中通入CO2:CO2+H2O+2ClOˉ═2HClO+CO32- | |
| B. | 向上述 NaClO溶液中通HF气体至恰好完全反应时:c(Na+)>c(F-)>c(HClO) | |
| C. | 在相同温度下,同浓度的三种酸溶液的导电能力顺序:H2CO3<HClO<HF | |
| D. | 若将CO2通入0.1mol•L-1Na2CO3溶液中至溶液中性,则溶液中2c(CO32-)+c (HCO3-)=0.1 mol•L-1 |
| A. | 乙烯为纯净物;聚乙烯为混合物 | |
| B. | 等质量的乙烯和聚乙烯完全燃烧后,生成的CO2和H2O的质量分别相等 | |
| C. | 乙烯的化学性质比聚乙烯活泼 | |
| D. | 乙烯和聚乙烯都能使溴水褪色 |
| A. | 1s22s12p5 | B. | 1s22s22p6 | C. | 1s22s22p63 s2 | D. | 1s22s22p63s1 |


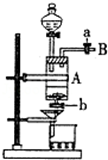 三氯化铁是中学化学实验室中常用的化学试剂.同学们利用废铁屑(含少量铜杂质)来探究制备FeCl3•6H2O的方法,同学甲设计的实验装置如图所示,其实验步骤如下:A中放有废铁屑,烧杯中盛有足量的稀硝酸,实验时先打开a并关闭b,用分液漏斗向A中加入过量的盐酸充分反应,此时溶液呈浅绿色;再打开b进行过滤,过滤结束后,取烧杯内溶液倒入蒸发皿加热,蒸发掉部分水并使剩余HNO3分解,再降温结晶得FeCl3•6H2O晶体.
三氯化铁是中学化学实验室中常用的化学试剂.同学们利用废铁屑(含少量铜杂质)来探究制备FeCl3•6H2O的方法,同学甲设计的实验装置如图所示,其实验步骤如下:A中放有废铁屑,烧杯中盛有足量的稀硝酸,实验时先打开a并关闭b,用分液漏斗向A中加入过量的盐酸充分反应,此时溶液呈浅绿色;再打开b进行过滤,过滤结束后,取烧杯内溶液倒入蒸发皿加热,蒸发掉部分水并使剩余HNO3分解,再降温结晶得FeCl3•6H2O晶体.