题目内容
13.下列电子排布式不属基态的是( )| A. | 1s22s12p5 | B. | 1s22s22p6 | C. | 1s22s22p63 s2 | D. | 1s22s22p63s1 |
分析 处于最低能量的原子叫做基态原子,基态电子排布遵循能量最低原理、泡利不相容原理和洪特规则,以此解答该题.
解答 解:A.1s22s12p5发生了电子跃迁,其基态原子的电子排布式应为1s22s22p4,故A正确;
B.1s22s22p6,符合基态电子排布规律,故B错误;
C.1s22s22p63s2,符合基态电子排布规律,故C错误;
D.1s22s22p63s1,符合基态电子排布规律,故D错误.
故选:A.
点评 本题考查核外电子排布,题目难度不大,注意基态电子排布规律与能量跃迁的关系.

练习册系列答案
 导学全程练创优训练系列答案
导学全程练创优训练系列答案
相关题目
3.下列溶液中粒子的物质的量浓度关系正确的是( )
| A. | 0.1 mol/L NaHCO3溶液与0.1 mol/L NaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-) | |
| B. | 20 mL 0.1 mol/L CH3COONa溶液与10 mL 0.1 mol/L HCl溶液混合后溶液呈酸性,所得溶液中:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+) | |
| C. | 室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)+c(H+)>c(NH4+)+c(OH-) | |
| D. | 0.1 mol/L CH3COOH溶液与0.1 mol/L NaOH溶液等体积混合,所得溶液中:c(OH-)>c(H+)+c(CH3COOH) |
1.标准状况下mg气体A和ngB气体的分子数相同,下列说法不正确的是( )
| A. | A与B的相对分子质量之比为m:n | |
| B. | 同温同压下,两气体A与B的密度之比为n:m | |
| C. | 同质量的A与B分子个数之比为m:n | |
| D. | 相同状况下,同体积的气体A与B 质量比为m:n |
18.已知氢化锂固体不导电,隔绝空气熔融时能导电,它跟水反应能生成氢气.下列有关氢化锂的说法中,错误的是( )
| A. | LiH是离子晶体 | B. | LiH的水溶液呈酸性 | ||
| C. | LiH是一种氧化剂 | D. | LiH中H-半径大于Li+半径 |
5.下列实验装置正确且能达到实验目的是( )
| A. | 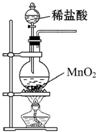 制取少量Cl2 | |
| B. | 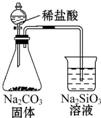 证明非金属性Cl>C>Si | |
| C. | 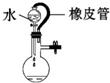 水不能持续流下,说明装置气密性良好 | |
| D. | 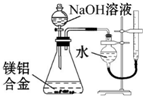 测定镁铝合金中铝的质量分数 |
2.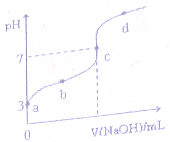 已知常温下CH3COOH的电离平衡常数为 k0,常温下,向20mL 0.1mol•L-1 CH3COOH溶液中逐滴加入0.1mol.L-1NaOH溶液,其 pH变化曲线如图所示(忽略温度变化).下列说法正确的是( )
已知常温下CH3COOH的电离平衡常数为 k0,常温下,向20mL 0.1mol•L-1 CH3COOH溶液中逐滴加入0.1mol.L-1NaOH溶液,其 pH变化曲线如图所示(忽略温度变化).下列说法正确的是( )
 已知常温下CH3COOH的电离平衡常数为 k0,常温下,向20mL 0.1mol•L-1 CH3COOH溶液中逐滴加入0.1mol.L-1NaOH溶液,其 pH变化曲线如图所示(忽略温度变化).下列说法正确的是( )
已知常温下CH3COOH的电离平衡常数为 k0,常温下,向20mL 0.1mol•L-1 CH3COOH溶液中逐滴加入0.1mol.L-1NaOH溶液,其 pH变化曲线如图所示(忽略温度变化).下列说法正确的是( )| A. | a点表溶液中由水电离出的温度为1.0xl0-3mol•L-1 | |
| B. | b 点表示的溶液 c (CH3COO-)<c (Na+) | |
| C. | b、d点表示的溶液中$\frac{c(C{H}_{3}COO)•c({H}^{+})}{c(C{H}_{3}COOH)}$相等 | |
| D. | c点表示CH3COOH和NaOH恰好反应完全 |
3.人们习惯上把金、银、铜、铁、锡五种金属统称为“五金”;在常温下,下列可以盛放在铁制容器中的物质是( )
| A. | 浓H2SO4 | B. | 稀HNO3 | C. | 盐酸 | D. | CuSO4溶液 |
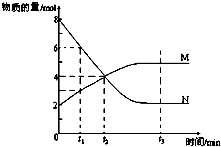 一定温度下,某容积为2L的密闭容器内,某一反应中M(g)、N(g)的物质的量随反应时间变化的曲线如图,依图所示:
一定温度下,某容积为2L的密闭容器内,某一反应中M(g)、N(g)的物质的量随反应时间变化的曲线如图,依图所示: