题目内容
8.下列有关说法正确的是( )| A. | 反应NH3(g)+HCl(g)═NH4Cl(s)在室温下可自发进行,则该反应的△H<0 | |
| B. | 电解法精炼铜时,以粗铜作阴极,纯铜作阳极 | |
| C. | CH3COOH 溶液加水稀释后,溶液中C(OH-)减小 | |
| D. | Na2CO3溶液中加入少量Ca(OH)2固体,CO32-水解程度减小,溶液的pH 减小 |
分析 A.依据反应自发进行的判断依据△H-T△S<0解答;
B.依据原电池原理解答;
C.醋酸加水稀释,促进醋酸电离,但溶液中氢离子浓度减小,温度不变,水的离子积常数不变,所以氢氧根离子浓度增大;
D.碳酸钠溶液中加入少量Ca(OH)2固体,二者反应生成碳酸钙和氢氧化钠,溶液的pH增大.
解答 解:A.反应NH3(g)+HCl(g)═NH4Cl(s)气体系数减小,△S<0,而反应能否自发进行即△H-T△S<0,所以,一定满足△H<0,故A正确;
B.电解法精炼铜时,以粗铜作阳极,纯铜作阴极,故B错误;
C.醋酸加水稀释,促进醋酸电离,但溶液中氢离子浓度减小,温度不变,水的离子积常数不变,所以氢氧根离子浓度增大,故C错误;
D.碳酸钠溶液中加入少量Ca(OH)2固体,二者反应生成碳酸钙和氢氧化钠,CO32-水解程度减小,溶液的pH增大,故D错误;
故选A.
点评 本题为综合题,考查了反应自发进行的判断依据、电解的应用、电离平衡移动影响因素、盐类水解,题目难度不大,注意弱电解质平衡移动影响因素以及平衡移动的方向的判断.

练习册系列答案
 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案
相关题目
7.下列关于二氧化硅的叙述正确的是( )
①可用于制造光导纤维
②能跟强碱反应,但不能与水反应
③SiO2的物理性质与CO2类似
④既是酸性氧化物,又是碱性氧化物.
①可用于制造光导纤维
②能跟强碱反应,但不能与水反应
③SiO2的物理性质与CO2类似
④既是酸性氧化物,又是碱性氧化物.
| A. | ①和② | B. | ③和④ | C. | ②和④ | D. | ②和③ |
3.对于在一定条件下进行的化学反应:2SO2+O2?2SO3,改变下列条件,可以提高反应物中的活化分子百分数的是( )
| A. | 升高温度 | B. | 增大压强 | C. | 减小反应物浓度 | D. | 增大反应物浓度 |
13.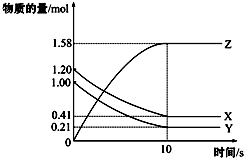 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:下列描述正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:下列描述正确的是( )
 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:下列描述正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:下列描述正确的是( )| A. | 反应开始到10 s,用Z表示的反应速率为0.158 mol/(L•s) | |
| B. | 反应开始到10 s,X的物质的量浓度减少了0.79 mol/L | |
| C. | 反应开始到10 s时,Y的转化率为79.0% | |
| D. | 在前10 s内用X、Y、Z表示的反应速率数值相等 |
20.下列化学用语正确的是( )
| A. | Cl-的结构示意图: | |
| B. | 金刚石、石墨互称为同素异形体 | |
| C. | 光导纤维主要成分的化学式:Si | |
| D. | H216O、D216O、H218O、D218O互为同位素 |
17.下列有机物的系统命名正确的是( )
| A. |  :3-甲基-2-戊烯 :3-甲基-2-戊烯 | B. |  :2-甲基-3-丁炔 :2-甲基-3-丁炔 | ||
| C. |  :1,3,4-三甲苯 :1,3,4-三甲苯 | D. | 2,3-二甲基-2-乙基己烷 |
18.下列物质中,能与氢氧化钠溶液反应,但不与盐酸反应的是( )
| A. | Al(OH)3 | B. | Al2O3 | C. | SiO2 | D. | Al |
 .
. .
.