题目内容
13.锂离子电池的应用很广,其正极材料可再生利用.某锂离子电池正极材料有钴酸锂(LiCoO2)、导电剂乙炔黑和铝箔等.充电时,该锂离子电池负极发生的反应为6C+xLi++xe-=LixC6.现欲利用以下工艺流程回收正极材料中的某些金属资源(部分条件未给出).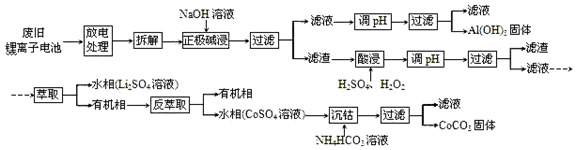
回答下列问题:
(1)“酸浸”一般在80℃下进行,写出该步骤中发生的所有氧化还原反应的化学方程式2LiCoO2+3H2SO4+H2O2$\frac{\underline{\;\;△\;\;}}{\;}$Li2SO4+2CoSO4+O2↑+4H2O;2H2O2$\frac{\underline{\;\;△\;\;}}{\;}$2H2O+O2↑ ;可用盐酸代替H2SO4和H2O2的混合液,但缺点是有氯气生成,污染较大.
(2)写出“沉钴”过程中发生反应的化学方程式CoSO4+2NH4HCO3=CoCO3↓+(NH4)2SO4+CO2↑+H2O.
(3)充放电过程中,发生LiCoO2与Li1-xCoO2之间的转化,写出充电时电池反应方程式LiCoO2+6C=Li1-xCoO2+LixC6.
(4)上述工艺中,“放电处理”有利于锂在正极的回收,其原因是Li+从负极中脱出,经由电解质向正极移动并进入正极材料中.在整个回收工艺中,可回收到的金属化合物有Al(OH)3、CoCO3、Li2SO4(填化学式).
分析 废旧锂离子电池放电处理拆解后正极用氢氧化钠溶液碱溶过滤得到滤液调节溶液PH过滤得到氢氧化铝沉淀;滤渣加入硫酸,过氧化氢调节溶液PH过滤得到滤液加入萃取剂萃取分液得到水层为硫酸锂,有机层通过反萃取得到水层硫酸钴溶液加入碳酸氢铵溶液沉淀钴离子得到碳酸钴固体;
(1)根据所加入的反应物以及生成物结合质量守恒定律来书写化学方程式;由题中信息知LiCoO2具有强氧化性,加入盐酸有污染性气体氯气生成;
(2)“沉钴”过程中硫酸钴和碳酸氢铵反应生成碳酸钴沉淀;
(3)充电时,LiCoO2和C发生氧化还原反应生成Li1-xCoO2和LixC6;
(4)“放电处理”有利于锂在正极的回收,Li+从负极中脱出,经由电解质向正极移动,在整个回收工艺中,可回收到的金属化合物有Al(OH)3、CoCO3、Li2SO4.
解答 解:(1)酸浸时反应物有硫酸、过氧化氢以及LiCoO2,生成物有Li2SO4和CoSO4,反应方程式为:2LiCoO2+3H2SO4+H2O2$\frac{\underline{\;\;△\;\;}}{\;}$Li2SO4+2CoSO4+O2↑+4H2O;2H2O2$\frac{\underline{\;\;△\;\;}}{\;}$2H2O+O2↑;由题中信息知LiCoO2具有强氧化性,加入盐酸有污染性气体氯气生成,污染较大;
故答案为:2LiCoO2+3H2SO4+H2O2$\frac{\underline{\;\;△\;\;}}{\;}$Li2SO4+2CoSO4+O2↑+4H2O;2H2O2$\frac{\underline{\;\;△\;\;}}{\;}$2H2O+O2↑;有氯气生成,污染较大;
(2)“沉钴”过程中硫酸钴和碳酸氢铵反应生成碳酸钴沉淀、硫酸铵、二氧化碳和水,反应方程式为CoSO4+2NH4HCO3=CoCO3↓+(NH4)2SO4+CO2↑+H2O;
故答案为:CoSO4+2NH4HCO3=CoCO3↓+(NH4)2SO4+CO2↑+H2O;
(3)充电时,LiCoO2和C发生氧化还原反应生成Li1-xCoO2和LixC6,反应方程式为:LiCoO2+6C=Li1-xCoO2+LixC6;
故答案为:LiCoO2+6C=Li1-xCoO2+LixC6;
(4)放电时,负极上生成锂离子,锂离子向正极移动并进入正极材料中,所以“放电处理”有利于锂在正极的回收,根据流程图知,可回收到的金属化合物有Al(OH)3、CoCO3、Li2SO4;
故答案为:Li+从负极中脱出,经由电解质向正极移动并进入正极材料中;Al(OH)3、CoCO3、Li2SO4.
点评 本题为生产流程题,涉及金属的回收、环境保护、氧化还原反应、电化学等问题,题目较为综合,做题时注意仔细审题,从题目中获取关键信息,难度中等.

| A | C | |
| B |
| A. | B为第二周期的元素 | B. | C为第五主族元素 | ||
| C. | A的原子序数为6 | D. | C是非金属性最强的元素 |
| A. | 贮氢金属并不是简单地吸附氢气,而是通过化学反应贮存氢气 | |
| B. | 物质变化中炭化、钝化、皂化、酯化、熔化都属于化学变化 | |
| C. | 石油分馏的馏分之一是石油气,石油气含有大量的己烷 | |
| D. | 使用煤液化的产品作燃料与直接燃烧煤比较,对保护环境有利,目前,煤液化的唯一途径是将煤在高温和催化剂条件下与氢气反应 |
| A. | CO32-+H+=HCO3- | B. | HCO3-+3CO32-+7H+═4CO2↑+4H2O | ||
| C. | 2HCO3-+5CO32-+12H+═7CO2↑+7H2O | D. | HCO3-+CO32-+3H+═2CO2↑+2H2O |
| A. | 使用清洁能源是防止酸雨发生的重要措施之一 | |
| B. | 推广“低碳经济”,减少温室气体的排放 | |
| C. | CO2、CH4、N2等均是造成温室效应的气体 | |
| D. | 利用晶体硅制作的太阳能电池可将太阳能直接转化为电能 |
| A. | 海水淡化------蒸馏 | |
| B. | 将碘单质从沙子提取出来--------过滤 | |
| C. | 盐水中获得食盐--------萃取分液 | |
| D. | 稀释浓硫酸时将水慢慢加入浓硫酸中 |
| A. | 参加反应的Fe2+全部作还原剂 | |
| B. | 生成1.5molFe3O4时,反应转移电子 6mol电子 | |
| C. | 方程式中a=2 | |
| D. | 反应中被氧化的元素是Fe,被还原的元素是S和O |
(1)常温下,浓度均为0.1mol•L-1的下列六种溶液的pH如下表:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
②根据表中数据判断,浓度均为0.01mol•L-1的下列四种物质的溶液中,酸性最强的是D;将各溶液分别稀释100倍,pH变化最小的是A(填编号).
A.HCN B.HClO C.H2CO3 D.CH3COOH
③据上表数据,请你判断下列反应不能成立的是C(填编号).
A.CH3COOH+Na2CO3═NaHCO3+CH3COONa
B.CH3COOH+NaCN═CH3COONa+HCN
C.CO2+H2O+2NaClO═Na2CO3+2HClO
④要增大氯水中HClO的浓度,可向氯水中加入少量的碳酸钠溶液,反应的离子方程式为2Cl2+CO32-+H2O=CO2↑+2Cl-+2HClO.
(2)已知常温下Cu(OH)2的Ksp=2×10-20.又知常温下某CuSO4溶液里c(Cu2+)=0.02mol•L-1,如果要生成Cu(OH)2沉淀,则应调整溶液pH大于5;要使0.2mol•L-1的CuSO4溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一)则应向溶液里加NaOH溶液,使溶液pH为6.
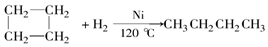
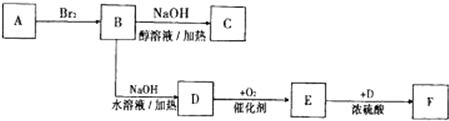
 ;C
;C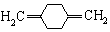 ;
;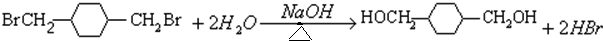 ;E→F:
;E→F: .
.