题目内容
17.银锌电池广泛用做各种电子仪器的电源,它的充电和放电过程可以表示为:2Ag+Zn(OH)2$?_{放电}^{充电}$Ag2O+Zn+H2O,在此电池放电时,正极上发生反应的物质是( )| A. | Ag | B. | Zn(OH)2 | C. | Ag2O | D. | Zn |
分析 2Ag+Zn(OH)2$?_{放电}^{充电}$Ag2O+Zn+H2O中,放电时,Zn失去电子,Ag得到电子,以此来解答.
解答 解:2Ag+Zn(OH)2$?_{放电}^{充电}$Ag2O+Zn+H2O中,放电时,Ag得到电子,则正极上发生反应的物质是Ag2O,
故选C.
点评 本题考查原电池工作原理,为高频考点,把握放电时为原电池及元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意原电池与氧化还原反应的关系,题目难度不大.

练习册系列答案
相关题目
7.向下列物质的溶液中加入浓氢氧化钠溶液并加热,产生能使湿润的红色石蕊试纸变蓝的气体,该物质是( )
| A. | MgCl2 | B. | KNO3 | C. | NaCl | D. | (NH4)2SO4 |
8.下列物质间离子方程式书写正确的是( )
| A. | 相同物质的量浓度的FeI2溶液与Br2水溶液等体积混合:2Fe2++2I-+2Br2═2Fe3++I2+4Br- | |
| B. | 向Ba(OH)2溶液中加入过量NH4HSO4溶液:NH4++Ba2++2OH-+H++SO42-═BaSO4↓+NH3•H2O+H2O | |
| C. | 向漂白粉溶液中通入过量的SO2:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO | |
| D. | 四氧化三铁溶于氢碘酸溶液中:Fe3O4+8H++2I-═3Fe2++I2+4H2O |
4.(1)已知反应:Na2S2O3+H2SO4═Na2SO4+S↓+SO2+H2O.甲同学通过测定该反应发生时溶液
变浑浊的时间,研究外界条件对化学反应速率的影响.设计实验如下:
其他条件不变时:探究温度对化学反应速率的影响,应选择实验②④(填实验编号);若同时选择实验①②、实验②③,测定混合液变浑浊的时间,可分别探究Na2S2O3浓度和H2SO4的浓度对化学反应速率的影响,则表中a和b分别为5.0和10.0.
(2)某同学设计如下实验流程探究Na2S2O3的化学性质.

实验操作①中测试时pH试纸的颜色应该接近D.
A.红色 B.黄色 C.深蓝色 D.绿色
上述流程中实验②、③的目的是为了探究Na2S2O3某种化学性质,你认为是探究了Na2S2O3的还原性.
变浑浊的时间,研究外界条件对化学反应速率的影响.设计实验如下:
| 实验编号 | 实验温度/℃ | c(Na2S2O3)/mol•L-1 | V(Na2S2O3)/mL | c(H2SO4)/mol•L-1 | V(H2SO4)/mL | V(H2O)/mL |
| ① | 25 | 0.1 | 5.0 | 0.1 | 10.0 | a |
| ② | 25 | 0.1 | 10.0 | 0.1 | 10.0 | 0 |
| ③ | 25 | 0.2 | 5.0 | 0.1 | 5.0 | b |
| ④ | 50 | 0.2 | 5.0 | 0.1 | 10.0 | 5.0 |
(2)某同学设计如下实验流程探究Na2S2O3的化学性质.

实验操作①中测试时pH试纸的颜色应该接近D.
A.红色 B.黄色 C.深蓝色 D.绿色
上述流程中实验②、③的目的是为了探究Na2S2O3某种化学性质,你认为是探究了Na2S2O3的还原性.
11.随着环保意识增强,清洁能源越来越受到人们关注.
(1)甲烷是一种理想的洁净燃料.已知:
CH4(g)+2O2(g)═CO2(g)+2H2O(g);△H=-802.3kJ•mol-1
H2O(1)═H2O(g),△H=+44.0kJ•mol-l
则4.8g甲烷气体完全燃烧生成液态水,放出的热量为267.1kJ.
(2)利用甲烷与水反应制备氢气,因原料廉价,具有推广价值.
该反应为CH4(g)+H2O(g)?CO(g)+3H2(g);△H=+206.1kJ•mol-l.
①若800℃时,反应的化学平衡常数K=l.0,某时刻测得该温度下密闭容器中各物质的物质的量浓度如下表.
则此时正、逆反应速率的关系是a.(填序号)
a.v(正)>v(逆) b.v(正)<v(逆)
c.v(正)=v(逆) d.无法判断
②为了探究温度、压强对上述化学反应速率的影响,某学习小组进行了以下三组对比实验(温度为360℃或480℃、压强为101kPa或303kPa,其余实验条件见下表).
表中P1=303,P2=101;
实验2、3的目的是探究温度对化学反应速率的影响.
实验1、2、3中反应的化学平衡常数的大小关系是K1=K3<K2 (用K1、K2、K3表示).
(1)甲烷是一种理想的洁净燃料.已知:
CH4(g)+2O2(g)═CO2(g)+2H2O(g);△H=-802.3kJ•mol-1
H2O(1)═H2O(g),△H=+44.0kJ•mol-l
则4.8g甲烷气体完全燃烧生成液态水,放出的热量为267.1kJ.
(2)利用甲烷与水反应制备氢气,因原料廉价,具有推广价值.
该反应为CH4(g)+H2O(g)?CO(g)+3H2(g);△H=+206.1kJ•mol-l.
①若800℃时,反应的化学平衡常数K=l.0,某时刻测得该温度下密闭容器中各物质的物质的量浓度如下表.
| CH4 (g) | H2O (g) | CO (g) | H2 (g) |
| 3.0mol•L-1 | 8.5mol•L-1 | 2.0mol•L-1 | 2.0mol•L-1 |
a.v(正)>v(逆) b.v(正)<v(逆)
c.v(正)=v(逆) d.无法判断
②为了探究温度、压强对上述化学反应速率的影响,某学习小组进行了以下三组对比实验(温度为360℃或480℃、压强为101kPa或303kPa,其余实验条件见下表).
| 实验序号 | 温度/℃ | 压强/kPa | V(CH4)/mol•L-1•s-1 | V(H2O)/mol•L-1•s-1 |
| 1 | 360 | P1 | 0.100 | 0.100 |
| 2 | 480 | 101 | 0.120 | 0.120 |
| 3 | 360 | P2 | 0.080 | 0.080 |
实验2、3的目的是探究温度对化学反应速率的影响.
实验1、2、3中反应的化学平衡常数的大小关系是K1=K3<K2 (用K1、K2、K3表示).
8.有机物甲可氧化生成羧酸,也可以还原生成醇.由甲生成的羧酸与醇在一定条件下反应可以生成化合物乙,其分子式为C2H4O2.下列叙述中正确的是( )
| A. | 甲分子中氢的质量分数为40% | |
| B. | 甲和由甲生成的羧酸与醇三者均可溶于水 | |
| C. | 甲在常温常压下为无色液体 | |
| D. | 乙和甲的最简式不同 |
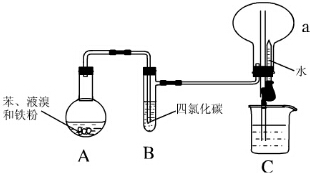 Ⅰ.某同学设计了如图所示的实验装置(夹持装置已略去)来研究苯和溴发生的反应.
Ⅰ.某同学设计了如图所示的实验装置(夹持装置已略去)来研究苯和溴发生的反应. .
. 现有纯铁片、纯银片、纯铜片,稀硫酸、FeSO4 溶液、Fe2(SO4)3溶液、U形管、导线若干,请运用原电池原理设计实验,验证Cu2+、Fe3+的氧化性强弱.
现有纯铁片、纯银片、纯铜片,稀硫酸、FeSO4 溶液、Fe2(SO4)3溶液、U形管、导线若干,请运用原电池原理设计实验,验证Cu2+、Fe3+的氧化性强弱.