题目内容
6.煤炭被人们誉为黑色的“金子”,它是人类使用的主要能源之一.为了提高煤的利用率,减少有害气体的排放,人们采取了各式各样的方法.(l)煤的气化和液化可以提高煤的利用率.煤的气化技术的主要产物是CO、H2.煤的液化又分为直接液化和间接液化.将煤隔绝空气加强热得到焦炉气、煤焦油及焦炭等产品的技术称为煤的干馏.
(2)煤在燃烧前后及燃烧过程中均可采取措施减少有害气体的排放
①在燃烧前,可以采用微生物脱硫技术.原理如图所示:
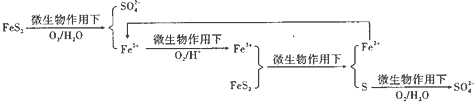
图示过程中Fe2+的作用为中间产物,催化剂作用,加快S元素的氧化.写出Fe2+$→_{O_{2}/H+}^{微生物}$Fe3+的离子方程式:4Fe2++O2+4H+$\frac{\underline{\;微生物\;}}{O_{2}/H+}$4Fe3++2H2O.
②煤在燃烧时,进行脱硫处理,常采用流化床燃烧技术,再把煤和脱硫剂加入锅炉燃烧室,使煤与空气在流化过程中充分混合、燃烧,起到固硫作用.常用脱硫剂的主要化学成分为CaO(填化学式).
③煤在燃烧后,烟气净化常采用除尘技术和脱硫、脱硝技术.湿法脱硫、脱硝技术中将烟气通入吸收塔设备,用石灰水淋洗.
分析 (1)煤的汽化是煤和水蒸气反应生成CO和氢气;将煤隔绝空气加强热使煤分解的操作是煤的干馏;
(2)①根据微生物脱硫技术的原理来分析;Fe2+做还原剂,被氧气氧化为Fe3+,氧气在酸性条件下被还原为H2O,据此写出离子方程式;
②在煤燃烧的同时进行的脱硫技术称为“流化床”燃烧技术;根据SO2是酸性氧化物来分析;
③吸收烟气的装置为吸收塔.
解答 解:(1)煤的汽化是煤和水蒸气在高温条件下反应生成CO和氢气的过程,故主要产物为CO、H2,煤的液化分为直接液化和间接液化,将煤隔绝空气加强热使煤分解得到焦炉气、煤焦油及焦炭等产品的操作是煤的干馏,故答案为:CO、H2;直接液化和间接液化;煤的干馏;
(2)①根据微生物脱硫技术的原理可知:Fe2+先被氧化为Fe3+,后Fe3+又被还原为Fe2+,即Fe2+先被消耗后又生成,故在反应中做催化剂;Fe2+做还原剂,被氧气氧化为Fe3+,氧气在酸性条件下被还原为H2O,据此写出离子方程式:4Fe2++O2+4H+$\frac{\underline{\;微生物\;}}{O_{2}/H+}$4Fe3++2H2O,故答案为:中间产物,催化剂作用,加快S元素的氧化;4Fe2++O2+4H+$\frac{\underline{\;微生物\;}}{O_{2}/H+}$4Fe3++2H2O;
②在煤燃烧的同时进行的脱硫技术称为“流化床”燃烧技术;由于SO2是酸性氧化物,故可以加碱性氧化物CaO(或者CaCO3)来加以吸收,故答案为:流化床;CaO(或者CaCO3);
③吸收烟气的装置为吸收塔,故答案为:吸收塔.
点评 本题考查二氧化硫的污染及治理,题目难度中等,本题注意从题目中获取信息,结合物质的性质解答.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
16. 苯甲酸(
苯甲酸(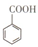 )和乙醇在浓硫酸催化下可以制得苯甲酸乙酯,及时除去反应中产生的水可提高酯的产率.据此某实验小组设计了如下图的装置来进行上述实验.相关信息如下:
)和乙醇在浓硫酸催化下可以制得苯甲酸乙酯,及时除去反应中产生的水可提高酯的产率.据此某实验小组设计了如下图的装置来进行上述实验.相关信息如下:
实验方案为:
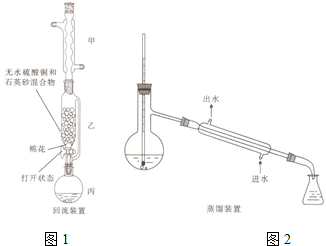
(1)仪器甲的名称为球形冷凝管.
(2)①往丙中加入药品的顺序为C.
A.无水乙醇、浓硫酸、苯甲酸晶体 B.浓硫酸、苯甲酸晶体、无水乙醇
C.苯甲酸晶体、无水乙醇、浓硫酸 D.苯甲酸晶体、浓硫酸、无水乙醇
②若加热反应后发现未加沸石,应采取的正确操作是停止加热,冷却后再加入沸石.
③微沸回流过程中,可以看到乙内的混合试剂的颜色变为蓝色.
(3)加入碳酸钠粉末的作用是中和浓硫酸及未反应的苯甲酸.
(4)分液要用到的玻璃仪器有分液漏斗、烧杯,粗产物在下层(填“上”或“下”).
(5)加热蒸馏若采用2图装置(加热装置已经略去)进行,该装置存在的2个问题为温度计的水银球不应插入反应液中、不应用直型冷凝管.
(6)本实验所得到的苯甲酸乙酯产率为80%.
(7)装置乙的作用为乙中的吸水剂可以吸收反应中产生的水分,有利于提高酯的产率.
 苯甲酸(
苯甲酸( )和乙醇在浓硫酸催化下可以制得苯甲酸乙酯,及时除去反应中产生的水可提高酯的产率.据此某实验小组设计了如下图的装置来进行上述实验.相关信息如下:
)和乙醇在浓硫酸催化下可以制得苯甲酸乙酯,及时除去反应中产生的水可提高酯的产率.据此某实验小组设计了如下图的装置来进行上述实验.相关信息如下:| 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 水中溶解度 | |
| 苯甲酸 | 122 | 1.27 | 249 | 微溶 |
| 乙醇 | 46 | 0.789 | 78.3 | 易溶 |
| 苯甲酸乙酯 | 150 | 1.05 | 212.6 | 难溶 |

(1)仪器甲的名称为球形冷凝管.
(2)①往丙中加入药品的顺序为C.
A.无水乙醇、浓硫酸、苯甲酸晶体 B.浓硫酸、苯甲酸晶体、无水乙醇
C.苯甲酸晶体、无水乙醇、浓硫酸 D.苯甲酸晶体、浓硫酸、无水乙醇
②若加热反应后发现未加沸石,应采取的正确操作是停止加热,冷却后再加入沸石.
③微沸回流过程中,可以看到乙内的混合试剂的颜色变为蓝色.
(3)加入碳酸钠粉末的作用是中和浓硫酸及未反应的苯甲酸.
(4)分液要用到的玻璃仪器有分液漏斗、烧杯,粗产物在下层(填“上”或“下”).
(5)加热蒸馏若采用2图装置(加热装置已经略去)进行,该装置存在的2个问题为温度计的水银球不应插入反应液中、不应用直型冷凝管.
(6)本实验所得到的苯甲酸乙酯产率为80%.
(7)装置乙的作用为乙中的吸水剂可以吸收反应中产生的水分,有利于提高酯的产率.
17.下列有关电解质溶液中微粒的物质的量浓度关系正确的是( )
| A. | 0.1mol•L-1(NH4)2Fe(SO4)2溶液中;c(NH4+)+c(NH3•H2O)+c(Fe2+)=0.3mol•L-1 | |
| B. | 常温下,pH=6的NaHSO3溶液中:c(SO32-)-c(H2SO3)=9.9×10-7mol•L-1 | |
| C. | NH4HSO3溶液中滴加NaOH至溶液恰好呈中性:c(Na+)>c(SO42-)=c(NH4+)>c(OH-)=c(H+) | |
| D. | 等浓度、等体积的Na2CO3和NaHCO3混合:$\frac{c(HC{{O}_{3}}^{-})}{c({H}_{2}C{O}_{3})}$>$\frac{c(C{{O}_{3}}^{2-})}{c(HC{{O}_{3}}^{-})}$ |
14. 汽车尾气中的主要污染物是NO和CO.为减轻大气污染,人们提出通过以下反应来处理汽车尾气:
汽车尾气中的主要污染物是NO和CO.为减轻大气污染,人们提出通过以下反应来处理汽车尾气:
(1)已知:2NO(g)+2CO(g)?2CO2(g)+N2(g)△H=-746.5KJ/mol(条件为使用催化剂)
2C (s)+O2(g)?2CO(g)△H=-221.0KJ/mol
C (s)+O2(g)?CO2(g)△H=-393.5KJ/mol
则N2(g)+O2(g)=2NO(g)△H=+180.5kJ•mol-1.
(2)T℃下,在一容积不变的密闭容器中,通入一定量的NO和CO,用气体传感器测得不同时间NO和CO的浓度如下表
则c1合理的数值为D(填字母标号).
A.4.20 B.4.00 C.3.50 D.2.50
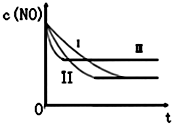
(3)研究表明:在使用等质量催化剂时,增大催化剂的比表面积可提高化学反应速率.根据下表设计的实验测得混合气体中NO的浓度随时间t变化的趋势如图所示:
则曲线I对应的实验编号为③.
(4)将不同物质的量的H2O(g)和CO(g)分别通入体积为2L的恒容密闭容器中,进行反应:H2O(g)+CO(g)?CO2(g)+H2(g),得到如下三组数据:
①实验组①中以v(CO2)表示的反应速率为0.16mol/(L•min).
②若a=2,b=1,则c=0.6,达平衡时实验组②中H2O(g)和实验组③中CO的转化率的关系为:α2 (H2O)=α3 (CO)(填“<”、“>”或“=”).
(5)CO分析仪的传感器可测定汽车尾气是否符合排放标准,该分析仪的工作原理类似于燃料电池,其中电解质是氧化钇(Y2O3)和氧化锆(ZrO2)晶体,能传导O2-.
①负极的电极反应式为CO+2O2--2e-=CO32-.
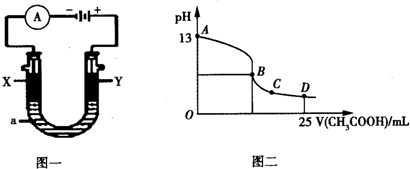
②以上述电池为电源,通过导线连接成图一.若X、Y为石墨,a为2L 0.1mol/L KCl溶液,写出电解总反应的离子方程式2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH-.电解一段时间后,取25mL上述电解后的溶液,滴加0.04mol/L醋酸得到图二曲线(不考虑能量损失和气体溶于水,溶液体积变化忽略不计).根据图二计算,上述电解过程中消耗一氧化碳的质量为2.8g.
 汽车尾气中的主要污染物是NO和CO.为减轻大气污染,人们提出通过以下反应来处理汽车尾气:
汽车尾气中的主要污染物是NO和CO.为减轻大气污染,人们提出通过以下反应来处理汽车尾气:(1)已知:2NO(g)+2CO(g)?2CO2(g)+N2(g)△H=-746.5KJ/mol(条件为使用催化剂)
2C (s)+O2(g)?2CO(g)△H=-221.0KJ/mol
C (s)+O2(g)?CO2(g)△H=-393.5KJ/mol
则N2(g)+O2(g)=2NO(g)△H=+180.5kJ•mol-1.
(2)T℃下,在一容积不变的密闭容器中,通入一定量的NO和CO,用气体传感器测得不同时间NO和CO的浓度如下表
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| C(NO)10-4 mol/L | 10.0 | 4.50 | C1 | 1.50 | 1.00 | 1.00 |
| C(CO)10-3 mol/L | 3.60 | 3.05 | C2 | 2.75 | 2.70 | 2.70 |
A.4.20 B.4.00 C.3.50 D.2.50
(3)研究表明:在使用等质量催化剂时,增大催化剂的比表面积可提高化学反应速率.根据下表设计的实验测得混合气体中NO的浓度随时间t变化的趋势如图所示:
| 实验 编号 | T/°C | NO初始浓 度/10-3mol•L-1 | CO初始浓 度/10-3mol•L-1 | 催化剂的比 表面积/m2•g-1 |
| ① | 350 | 1.20 | 5.80 | 124 |
| ② | 280 | 1.20 | 5.80 | 124 |
| ③ | 280 | 1.20 | 5.80 | 82 |
(4)将不同物质的量的H2O(g)和CO(g)分别通入体积为2L的恒容密闭容器中,进行反应:H2O(g)+CO(g)?CO2(g)+H2(g),得到如下三组数据:
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所 需时间/min | ||
| H2O | CO | CO | H2 | |||
| ① | 650 | 2 | 4 | 2.4 | 1.6 | 5 |
| ② | 900 | 1 | 2 | 1.6 | 0.4 | 3 |
| ③ | 900 | a | b | c | d | t |
②若a=2,b=1,则c=0.6,达平衡时实验组②中H2O(g)和实验组③中CO的转化率的关系为:α2 (H2O)=α3 (CO)(填“<”、“>”或“=”).
(5)CO分析仪的传感器可测定汽车尾气是否符合排放标准,该分析仪的工作原理类似于燃料电池,其中电解质是氧化钇(Y2O3)和氧化锆(ZrO2)晶体,能传导O2-.
①负极的电极反应式为CO+2O2--2e-=CO32-.

②以上述电池为电源,通过导线连接成图一.若X、Y为石墨,a为2L 0.1mol/L KCl溶液,写出电解总反应的离子方程式2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH-.电解一段时间后,取25mL上述电解后的溶液,滴加0.04mol/L醋酸得到图二曲线(不考虑能量损失和气体溶于水,溶液体积变化忽略不计).根据图二计算,上述电解过程中消耗一氧化碳的质量为2.8g.
1.下列关于化学素养的说法中,正确的是( )
| A. | 海水中含有丰富的碘元素,故碘被称为“海洋元素” | |
| B. | 溴化银是一种重要的感光材料,也可用于人工降雨 | |
| C. | 钠在盛有氯气的集气瓶中燃烧,火焰呈苍白色,产物为NaCl;铁在盛有氯气的集气瓶中燃烧,火焰呈棕黄色,产物为FeCl3 | |
| D. | 工业炼铁的设备是炼铁高炉,过程中加入石灰石的作用是除脉石(SiO2)造渣 |
11.根据下列物质的化学性质,判断其应用错误的是( )
| A. | 镁燃烧发出耀眼的白光,可用来制造信号弹和焰火 | |
| B. | 碳酸氢钠能与酸反应,可用来治疗胃酸过多 | |
| C. | 利用铜与氯化铁溶液的反应来制作印刷电路板 | |
| D. | 铝制品表面有致密的氧化膜保护层,可长时间盛放咸菜等腌制食品 |
18.Fe2O3在工业上有重要的用途,可发生如图所示的一系列反应.下列说法正确的是( )
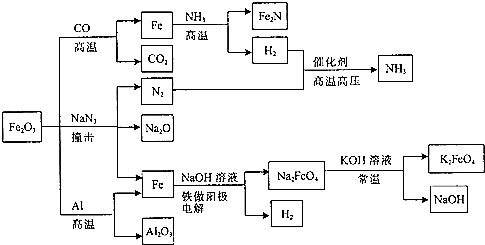

| A. | Fe2O3与Al的反应属于吸热反应 | |
| B. | Fe2O3与NaN3反应,每消耗1molFe2O3产生9molN2 | |
| C. | Fe2O3与CO的反应属于置换反应 | |
| D. | 常温下K2FeO4在水中的溶解度比Na2FeO4的大 |
16.已知三氧化硫的熔点为16.8℃,沸点为44℃,下列有关三氧化硫的说法中,正确的是( )
| A. | 常温下SO3是液体 | |
| B. | 标准状况下,1 mol SO3的体积约为22.4L | |
| C. | SO3与CaO反应生成CaSO3 | |
| D. | SO2遇空气即生成SO3 |
 ;
;