题目内容
常温下,100ml 蒸馏水中加入0.1mol CH3COONa ,下列说法正确的是
| A.该溶液中存在: c(Na+) + c(H+)=c(OH—)+c(CH3COO—) |
| B.加入酚酞后加热,溶液颜色变浅 |
| C.若在该溶液再通入0.1mol HCl,存在: c(Na+)>c(CH3COO—)> c(H+) |
| D.若在该溶液中再投入0.1mol NaCl,存在: c(Na+)=c(Cl—)+c(CH3COO—)+c(CH3COOH) |
AD
试题分析:由已知条件配成的醋酸钠溶液,有电荷守恒式c(Na+) + c(H+)=c(OH—)+c(CH3COO—) ,所以A正确;醋酸钠溶液水解呈碱性,加热溶液促进水解,碱性增强,所以酚酞应该变红,B错误;若在该溶液再通入0.1mol HCl,则CH3COONa+ HCl=CH3COOH+NaCl,所以所得溶液为CH3COOH和NaCl的混合溶液,所以醋酸发生电离得到的c(CH3COO—)=c(H+),又水电离出一部分H+,所以c(CH3COO—)<c(H+),C错误;往溶液中投入0.1mol NaCl,根据物料守恒有c(Na+)=c(Cl—)+c(CH3COO—) +c(CH3COOH),所以D正确;故选AD。

练习册系列答案
 小学课时特训系列答案
小学课时特训系列答案
相关题目
 )
) )>c(HC
)>c(HC )
)
 >
> >
>
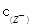 /
/ ·
· 的比值变小,若加少量盐酸,则比值变大
的比值变小,若加少量盐酸,则比值变大 <
<
 >
> >
> 比值增大
比值增大 是弱电解质的是
是弱电解质的是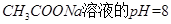
 溶液的pH=2.8
溶液的pH=2.8 溶液与稀盐酸反应生成
溶液与稀盐酸反应生成