题目内容
下列关于钢铁的析氢腐蚀的说法中正确的是( )
| A、铁为正极 |
| B、碳为正极 |
| C、溶液中氢离子浓度不变 |
| D、析氢腐蚀在任何溶液中都会发生 |
考点:金属的电化学腐蚀与防护
专题:
分析:强酸性条件下,钢铁中C、Fe和酸构成原电池,Fe易失电子发生氧化反应而作负极、C作正极,正极上氢离子得电子发生还原反应,据此分析解答.
解答:
解:强酸性条件下,钢铁中C、Fe和酸构成原电池,Fe易失电子发生氧化反应而作负极、C作正极,负极反应式为Fe-2e-=Fe2+,正极反应式为2H++2e-=H2↑,
A.Fe作负极、C作正极,故A错误;
B.C作正极、Fe作负极,故B正确;
C.正极反应式为2H++2e-=H2↑,所以溶液中氢离子浓度减小,故C错误;
D.强酸性条件下钢铁发生析氢腐蚀,弱酸性或中性条件下,钢铁发生吸氧腐蚀,故D错误;
故选B.
A.Fe作负极、C作正极,故A错误;
B.C作正极、Fe作负极,故B正确;
C.正极反应式为2H++2e-=H2↑,所以溶液中氢离子浓度减小,故C错误;
D.强酸性条件下钢铁发生析氢腐蚀,弱酸性或中性条件下,钢铁发生吸氧腐蚀,故D错误;
故选B.
点评:本题考查钢铁的析氢腐蚀,明确析氢腐蚀及吸氧腐蚀区别是解本题关键,知道钢铁发生析氢腐蚀及吸氧腐蚀的条件,会正确书写各个电极上电极反应式,题目难度不大.

练习册系列答案
相关题目
下列事实不能用勒夏特列原理解释的是( )
| A、黄绿色的氯水光照后颜色变浅 |
| B、NO2(g)+SO2(g)?SO3(g)+NO(g),对该平衡体系加压后颜色加深 |
| C、由NO2和N2O4组成的平衡体系加压后颜色先变深后变浅 |
| D、在含有Fe(SCN)3的红色溶液中加铁粉,振荡静置,溶液颜色变浅或褪去 |
下列根据反应原理设计的应用,不正确的是( )
| A、CO32-+H2O?HCO3-+OH- Na2CO3与Al2(SO4)3溶液混合作灭火剂 |
| B、Al3++3H2O?Al(OH)3+3H+ 明矾净水 |
| C、TiCl4+(x+2)H2O(过量)?TiO2?xH2O↓+4HCl 制备TiO2纳米粉 |
| D、SnCl2+H2O?Sn(OH)Cl↓+HCl 配制氯化亚锡溶液时加入浓盐酸 |
某有机物A的分子式为C6H12O2,已知A~E有如图转化关系.则A的结构可能有( )
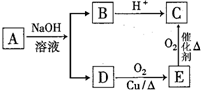

| A、1种 | B、2种 | C、3种 | D、4种 |
 (1)可用如图示的方法表示不同反应类型之间的关系.如分解反应和氧化还原反应可表示为如图.请在下面的方框中画出离子反应、置换反应和氧化还原反应三者之间的关系.
(1)可用如图示的方法表示不同反应类型之间的关系.如分解反应和氧化还原反应可表示为如图.请在下面的方框中画出离子反应、置换反应和氧化还原反应三者之间的关系.