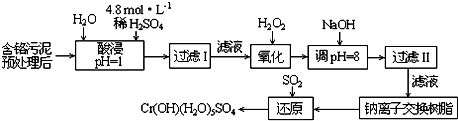
题目内容
 乙酰苯胺是一种白色有光泽片状结晶或白色结晶粉末,是磺胺类药物的原料,可用作止痛剂、退热剂、防腐剂和染料中间体.乙酰苯胺的制备原理为:
乙酰苯胺是一种白色有光泽片状结晶或白色结晶粉末,是磺胺类药物的原料,可用作止痛剂、退热剂、防腐剂和染料中间体.乙酰苯胺的制备原理为: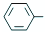 NH2+CHC3OOH?
NH2+CHC3OOH?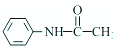 -H2O
-H2O实验参数:
| 名称 | 性状 | 密度/(g/cm3) | 沸点/℃ | 溶解性 | |
| 苯胺 | 无色油状液体,有还原性 | 1.02 | 184.4 | 微溶于水 | 易溶于乙醇、乙醚等 |
| 乙酸 | 无色液体 | 1.05 | 118.1 | 易溶于水 | 易溶于乙醇、乙醚 |
| 乙酰苯胺 | 白色晶体 | 1.22 | 304 | 微溶于冷水,溶于热水 | 易溶于乙醇、乙醚 |
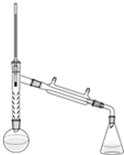
注:刺形分馏柱的作用相当于二次蒸馏,用于沸点差别不太大的混合物的分离.
实验步骤:
步骤1:在圆底烧瓶中加入无水苯胺9.3mL,冰醋酸18.4mL,锌粉0.1g,安装仪器,加入沸石,调节加热温度,使柱顶温度控制在105℃左右,反应约60~80min,反应生成的水及少量醋酸被蒸出.
步骤2:在搅拌下,趁热将烧瓶中的物料以细流状倒入盛有100mL冰水的烧杯中,剧烈搅拌,并冷却,结晶,抽滤、洗涤、干燥,得到乙酰苯胺粗品.
步骤3:将此粗乙酰苯胺进行重结晶,晾干,称重,计算产率.
请回答下列问题:
(1)步骤1中所选圆底烧瓶的最佳规格是
a.25mL b.50mL c.150mL d.200mL
(2)从化学平衡的角度分析,要控制分馏柱上端的温度在105℃左右的原因是
(3)步骤1加热可用
(4)洗涤乙酰苯胺粗品最合适的试剂是
a.用少量冷水洗 b.用少量热水洗c.先用冷水洗,再用热水洗 d.用酒精洗
(5)步骤2得到的粗晶体中因含有某些杂质而颜色较深,步骤3重结晶的操作是:将粗晶体用热水溶解,加入活性炭0.1g,煮沸进行脱色,
(6)该实验最终得到纯品9.1g,已知苯胺、乙酸和乙酰苯胺的摩尔质量分别为93g?mol-1、60g?mol-1、135g?mol-1.则乙酰苯胺的产率是
考点:制备实验方案的设计
专题:实验设计题
分析:(1)圆底烧瓶中盛放液体的体积不超过容积的
分析判断;
(2)水的沸点是100℃,加热至105℃左右,就可以不断分出反应过程中生成的水,促进反应正向进行;
(3)由于步聚1加热的温度在105℃左右,而沸腾的水温度为100℃,不能达到该温度,所以步骤1可用油浴加热的方法;
(4)由于乙酰苯胺微溶于冷水,溶于热水,所以洗涤粗品最合适的试剂是用少量冷水洗,以减少因洗涤造成的损耗;
(5)避免过滤过程中损失,趁热过滤;
(6)计算苯胺、乙酸的物质的量,判断反应物过量问题,根据不足量的物质计算乙酰苯胺的理论产量,进而计算乙酰苯胺的产率.
| 2 |
| 3 |
(2)水的沸点是100℃,加热至105℃左右,就可以不断分出反应过程中生成的水,促进反应正向进行;
(3)由于步聚1加热的温度在105℃左右,而沸腾的水温度为100℃,不能达到该温度,所以步骤1可用油浴加热的方法;
(4)由于乙酰苯胺微溶于冷水,溶于热水,所以洗涤粗品最合适的试剂是用少量冷水洗,以减少因洗涤造成的损耗;
(5)避免过滤过程中损失,趁热过滤;
(6)计算苯胺、乙酸的物质的量,判断反应物过量问题,根据不足量的物质计算乙酰苯胺的理论产量,进而计算乙酰苯胺的产率.
解答:
解:(1)由于苯胺不稳定,容易被空气中的氧气氧化为硝基苯,加入还原剂Zn粉,可以防止苯胺在反应过程中被氧化,故答案为:防止苯胺在反应过程中被氧化;
(2)水的沸点是100℃,加热至105℃左右,就可以不断分出反应过程中生成的水,促进反应正向进行,提高生成物的产率;
故答案为:不断分出反应过程中生成的水,促进反应正向进行,提高生成物的产率;
(3)由于步聚1加热的温度在105℃左右,而沸腾的水温度为100℃,不能达到该温度,所以步骤1可用油浴加热的方法;
故答案为:油浴;
(4)由于乙酰苯胺微溶于冷水,溶于热水,易溶于乙醇、乙醚,所以洗涤粗品最合适的试剂是用少量冷水洗,以减少因洗涤造成的损耗,
故选:a;
步骤2得到的粗晶体中因含有某些杂质而颜色较深,步骤3重结晶的操作是:将粗晶体用热水溶解,加入活性炭0.1g,煮沸进行脱色,趁热过滤减少晶体的损耗,再将滤液冷却结晶;
故答案为:趁热过滤;
(6)n(苯胺)=
=0.102mol,n(乙酸)=( 18.4mL×1.05g/ml)÷60g/mol=0.322ol,二者按1:1反应,由于乙酸的物质的量大于苯胺的物质的量,所以产生乙酰苯胺的物质的量要以不足量的苯胺为原料为标准,乙酰苯胺的理论产量为0.102mol,而实际产量n(乙酰苯胺)=9.1g÷135g/mol=0.067mol,所以乙酰苯胺的产率为(0.06mol÷0.1mol)
×100%=66%,
故答案为:66%.
(2)水的沸点是100℃,加热至105℃左右,就可以不断分出反应过程中生成的水,促进反应正向进行,提高生成物的产率;
故答案为:不断分出反应过程中生成的水,促进反应正向进行,提高生成物的产率;
(3)由于步聚1加热的温度在105℃左右,而沸腾的水温度为100℃,不能达到该温度,所以步骤1可用油浴加热的方法;
故答案为:油浴;
(4)由于乙酰苯胺微溶于冷水,溶于热水,易溶于乙醇、乙醚,所以洗涤粗品最合适的试剂是用少量冷水洗,以减少因洗涤造成的损耗,
故选:a;
步骤2得到的粗晶体中因含有某些杂质而颜色较深,步骤3重结晶的操作是:将粗晶体用热水溶解,加入活性炭0.1g,煮沸进行脱色,趁热过滤减少晶体的损耗,再将滤液冷却结晶;
故答案为:趁热过滤;
(6)n(苯胺)=
| 9.3ml×1.02g/ml |
| 93g/mol |
| 0.067mol |
| 0.102mol |
故答案为:66%.
点评:本题考查有机物的合成实验、基本操作、实验条件的控制与分析评价等,是对学生综合能力的考查,需要学生具备扎实的基础,难度中等.

练习册系列答案
相关题目
下列说法中正确的是( )
| A、航天飞机上的隔热陶瓷瓦属于优质合金材料 |
| B、将少量CO2通入CaCl2溶液能生成白色沉淀 |
| C、蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有吸水性 |
| D、碱性氧化物一定是金属氧化物,金属氧化物不一定是碱性氧化物 |
下列变化属于化学变化,且产物中兼有气体、液体、固体的是( )
| A、石油的分馏 | B、石油的裂解 |
| C、煤的干馏 | D、煤的气化 |
下列溶液中微粒的物质的量浓度关系正确的是( )
| A、25℃时,等体积、等浓度的NaX和弱酸HX混合后的溶液中:c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-) |
| B、常温下,pH≈5.5的0.1mol/LNaHC2O4溶液:c(Na+)>c(HC2O4-)>c(H2C2O4)>c(C2O42-) |
| C、0.1mol/LNaHS溶液:c(OH-)+c(S2-)=c(H+)+c(H2S) |
| D、室温下,向0.1mol/LNH4HSO4溶液中滴加NaOH溶液至中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) |
下列有关有机化合物的叙述正确的是( )
| A、进入人体的重金属盐能使蛋白质变性,所以会使人中毒 |
| B、卤代烃C4H8Cl2有四种同分异构体 |
| C、甲烷是天然气的主要成分,能发生加成反应 |
| D、用驴皮熬制成的胶(阿胶)是一种天然橡胶,属于天然高分子化合物 |
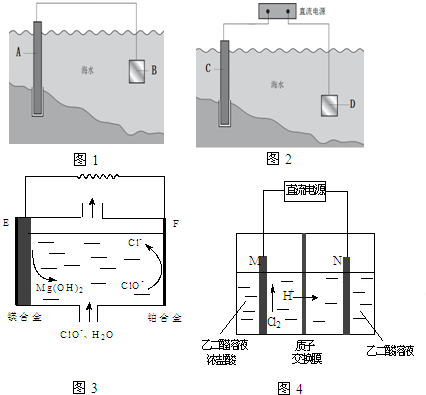 电化学原理在防止金属腐蚀、能量转换、物质合成等方面应用广泛.
电化学原理在防止金属腐蚀、能量转换、物质合成等方面应用广泛.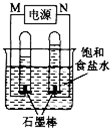 CO和H2作为重要的燃料和化工原料,有着十分广泛的应用.
CO和H2作为重要的燃料和化工原料,有着十分广泛的应用.