题目内容
一定量的氢气在氯气中燃烧,所得混合物用100mL 3.00mol?L-1的NaOH溶液恰好完全吸收,测得溶液中含有NaClO的物质的量为0.10mol.
(1)上述变化中涉及三个化学反应,其中一个反应为H2+Cl2
2HCl,请写出另外两个反应的离子方程式: 、 .
(2)参加反应的氢气和氯气的物质的量之比n(H2) n(Cl2)为 .
(3)工业制取漂白粉的原料是氯气和石灰乳,漂白粉的有效成分为 .
(1)上述变化中涉及三个化学反应,其中一个反应为H2+Cl2
| ||
(2)参加反应的氢气和氯气的物质的量之比n(H2) n(Cl2)为
(3)工业制取漂白粉的原料是氯气和石灰乳,漂白粉的有效成分为
考点:化学方程式的有关计算
专题:
分析:(1)氢气在氯气中燃烧生成氯化氢气体,盐酸可以和氢氧化钠之间发生中和反应,氯气可以和强碱之间反应生成氯化钠、次氯酸钠和水;
(2)根据次氯酸钠的物质的量,计算反应Cl2+2NaOH=NaCl+NaClO+H2O中氯气、氢氧化钠物质的量,进而计算与HCl反应的NaOH,再根据H2+Cl2
2HCl计算该反应中消耗氢气与氯气的物质的量;
(3)漂白粉的有效成分是次氯酸钙.
(2)根据次氯酸钠的物质的量,计算反应Cl2+2NaOH=NaCl+NaClO+H2O中氯气、氢氧化钠物质的量,进而计算与HCl反应的NaOH,再根据H2+Cl2
| ||
(3)漂白粉的有效成分是次氯酸钙.
解答:
解:(1)盐酸可以和氢氧化钠之间发生中和反应,离子方程式为:H++OH-=H2O,氯气可以和强碱之间反应生成氯化钠、次氯酸钠和水,离子方程式为:Cl2+2OH-=Cl-+ClO-+H2O,
故答案为:H++OH-=H2O;Cl2+2OH-=Cl-+ClO-+H2O;
(2)NaClO的物质的量为0.10mol,根据Cl2+2NaOH=NaCl+NaClO+H2O,可知消耗的氯气为0.1mol,消耗NaOH的物质的量为0.20mol,故与HCl反应的NaOH为0.1L×3mol/L-0.2mol=0.1mol,故HCl为0.1mol,由可知H2+Cl2
2HCl,该反应中氢气为0.05mol,氯气为0.05mol,故氯气的总物质的量是0.15mol,参加反应的n(H2):n(Cl2)=0.05mol:0.15mol=1:3,
故答案为:1:3;
(3)漂白粉的成分为氯化钙、次氯酸钙,有效成分是次氯酸钙,故答案为:Ca(ClO)2(或次氯酸钙).
故答案为:H++OH-=H2O;Cl2+2OH-=Cl-+ClO-+H2O;
(2)NaClO的物质的量为0.10mol,根据Cl2+2NaOH=NaCl+NaClO+H2O,可知消耗的氯气为0.1mol,消耗NaOH的物质的量为0.20mol,故与HCl反应的NaOH为0.1L×3mol/L-0.2mol=0.1mol,故HCl为0.1mol,由可知H2+Cl2
| ||
故答案为:1:3;
(3)漂白粉的成分为氯化钙、次氯酸钙,有效成分是次氯酸钙,故答案为:Ca(ClO)2(或次氯酸钙).
点评:本题考查混合物有关计算等,难度不大,明确发生的反应是关键,注意对基础知识的理解掌握.

练习册系列答案
相关题目
关于原电池和电解池的电极名称,下列说法错误的是( )
| A、原电池中失去电子的一极一定为负极 |
| B、电解池中与直流电源负极相连的一极一定为阴极 |
| C、电解池中发生氧化反应的一极一定为阳极 |
| D、原电池中负极的质量一定减少 |
在下列反应中,水仅作还原剂的是( )
| A、Na2O+H2O=2NaOH | ||||
| B、2F2+2H2O=4HF+O2 | ||||
| C、C+H2O=CO+H2 | ||||
D、2H2O
|
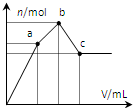 向100mL 0.1mol?L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1mol?L-1 Ba(OH)2溶液.随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示.下列说法正确的( )
向100mL 0.1mol?L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1mol?L-1 Ba(OH)2溶液.随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示.下列说法正确的( )| A、a点的溶液呈中性 |
| B、a点沉淀的质量比c点沉淀的质量大 |
| C、b点加入Ba(OH)2溶液的体积为250 mL |
| D、至c点完成反应,反应的离子方程式可表示为:Al3++2SO42-+NH4++2Ba2++5OH-→AlO2-+2BaSO4↓+NH3?H2O+2H2O |
用NA表示阿伏加德罗常数的值.下列说法不正确的是( )
| A、0.5molCl2与铁反应转移电子数为NA |
| B、在标准状况下,NA个任何分子所占的体积均约为22.4L |
| C、300mL 5mol/L KNO3溶液与300mL 5mol/L KCl溶液含有的离子数均约为3NA |
| D、16gO2和O3中所含的氧原子数均为NA |
下列离子方程式书写正确的是( )
| A、稀硝酸溶液中加入氢氧化亚铁:Fe(OH)2+2H+=Fe2++2H2O |
| B、NaOH溶液中加入过量Ba(HCO3)2溶液:Ba2++2OH-+2HCO3-=BaCO3↓+2H2O+CO32- |
| C、FeI2溶液中通入极少量Cl2:2I-+Cl2=I2+2Cl- |
| D、AlCl3溶液中加入过量氨水:Al3++4OH-=AlO2-+2H2O |
下列说法正确的是( )
A、相同条件下,结合质子的能力:OH->AlO2->CO32->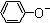 >HCO3->CH3COO- >HCO3->CH3COO- |
B、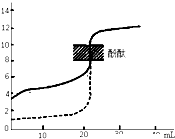 如图表示用0.1mol/LNaOH溶液分别滴定相同物质的量浓度和相同体积的盐酸和醋酸,其中实线表示的是滴定盐酸的曲线 |
| C、一定条件下,使用催化剂能加快反应速率并提高反应物的平衡转化率,平衡常数保持不变 |
| D、恒容密闭容器中进行的反应A(g)?B(g)+C(g),在其它条件不变情况下,再充入一定量的A气体,A的转化率将增大 |
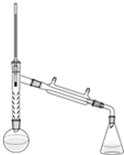 乙酰苯胺是一种白色有光泽片状结晶或白色结晶粉末,是磺胺类药物的原料,可用作止痛剂、退热剂、防腐剂和染料中间体.乙酰苯胺的制备原理为:
乙酰苯胺是一种白色有光泽片状结晶或白色结晶粉末,是磺胺类药物的原料,可用作止痛剂、退热剂、防腐剂和染料中间体.乙酰苯胺的制备原理为: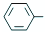 NH2+CHC3OOH?
NH2+CHC3OOH?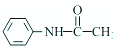 -H2O
-H2O