题目内容
将乙烷和乙烯的混合气体通过装有溴水的试剂瓶,试剂瓶质量增加了5.6克,则吸收的乙烯在标准状况下的体积是( )
| A、2.24L |
| B、4.48L |
| C、6.40L |
| D、12.8L |
考点:有关混合物反应的计算
专题:计算题
分析:乙烯与溴水发生加成反应,而乙烷与溴水不反应,故溴水增重5.6g为乙烯的质量,根据n=
计算乙烯的物质的量,再根据V=nVm计算乙烯的体积.
| m |
| M |
解答:
解:乙烯与溴水发生加成反应,而乙烷与溴水不反应,故溴水增重5.6g为乙烯的质量,则乙烯的物质的量为
=0.2mol,标况下乙烯的体积为0.2mol×22.4L/mol=4.48L,故选B.
| 5.6g |
| 28g/mol |
点评:本题考查混合物计算、烃的性质等,题目贴近教材,基础性强,明确乙烷与乙烯性质的不同即可解答.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
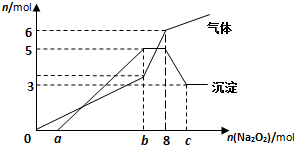 将Na2O2逐渐加入到含有H+、Mg2+、Al3+、NH4+的混合液中并微热,产生沉淀和气体的物质的量(mol)与加入的
将Na2O2逐渐加入到含有H+、Mg2+、Al3+、NH4+的混合液中并微热,产生沉淀和气体的物质的量(mol)与加入的Na2O2物质的量(mol)的关系如图所示,则原溶液中的
Mg2+、Al3+、NH4+物质的量分别为( )
| A、2mol、3mol、6mol |
| B、3mol、2mol、6mol |
| C、2mol、3mol、4mol |
| D、3mol、2mol、2mol |
将14g金属的混合物投入足量的盐酸中,反应完全后得到氢气11.2L(标准状况),该混合物的组成可能是( )
| A、钙和锌 | B、镁和铜 |
| C、铝和镁 | D、锌和铁 |
关于电解CuCl2溶液实验说法正确的是( )
| A、溶液中Cu2+向阳极移动,Cl-向阴极移动 |
| B、阳极上发生还原反应,阴极上发生氧化反应 |
| C、阴极反应:Cu2++2e-=Cu |
| D、可以用湿润的KI淀粉试纸检验阴极产生气体为Cl2 |
用惰性电极电解下列物质的水溶液时,在阳极上不生成O2的是( )
| A、NaOH |
| B、H2SO4 |
| C、ZnCl2 |
| D、Na2SO4 |
下列实验过程中,始终无明显现象的是( )
| A、NO2通入FeSO4溶液中 |
| B、CO2通入CaCl2溶液中 |
| C、Cl2通入Na2CO3溶液中 |
| D、向Na2SiO3溶液中通入过量的CO2气体 |
一定温度下将1mol CO和1mol H2O(g)通入一个密闭容器中反应:CO(g)+H2O(g)═CO2(g)+H2(g),达到平衡后CO2的物质的量为
mol.在相同条件下,若将1mol CO2、1mol H2、1mol H2O(g)同时通入同一个密闭容器中反应,达到平衡后CO2的体积分数可能是( )
| 2 |
| 3 |
| A、22.2% |
| B、27.5% |
| C、33.3% |
| D、36.8% |
下列分子或离子在指定的分散系中能大量共存的一组是( )
| A、银氨溶液:Na+、K+、NO3-、NH3?H2O |
| B、空气:C2H2、CO2、SO2、NO |
| C、氢氧化铁胶体:H+、K+、S2-、Br- |
| D、高锰酸钾溶液:H+、Na+、SO42-、葡萄糖分子 |
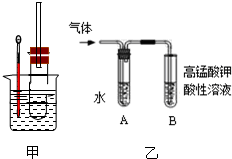 某学习小组用乙醇与氢溴酸为原料制备溴乙烷.该反应发生的原理为:C2H5OH+HBr
某学习小组用乙醇与氢溴酸为原料制备溴乙烷.该反应发生的原理为:C2H5OH+HBr