题目内容
下列实验操作,能有效改变反应速率且达到变化要求的是( )
| A、为增大泡沫灭火器中Al2(SO4)3与小苏打的反应速率,改用小苏打和苏打的混合物 |
| B、为加快盐酸和锌制取氢气的速率又不减少氢气的量,可加少量硝酸银溶液 |
| C、在稀硫酸和铁粉反应制取氢气时,为减慢反应速率,可以加入适量醋酸钠 |
| D、用3 mL乙醇、2 mL浓H2SO4、2 mL冰醋酸制乙酸乙酯,为增大反应速率,可改用6 mL乙醇、4 mL浓H2SO4、4 mL冰醋酸 |
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:A、根据产生二氧化碳的原理以及影响反应速率的因素来回答;
B、硝酸银和盐酸之间反应生成氯化银沉淀和硝酸;
C、醋酸钠可以和硫酸之间反应生成硫酸钠和醋酸,强酸制得弱酸;
D、增加物质的体积不会增大物质的量浓度.
B、硝酸银和盐酸之间反应生成氯化银沉淀和硝酸;
C、醋酸钠可以和硫酸之间反应生成硫酸钠和醋酸,强酸制得弱酸;
D、增加物质的体积不会增大物质的量浓度.
解答:
解:A、泡沫灭火器主要是利用铝离子和碳酸氢根离子发生双水解反应产生二氧化碳的原理,用碳酸钠和碳酸氢钠的混合物,铝离子和碳酸根离子也会双水解,但是速率变化不大,故A错误;
B、盐酸和锌制取氢气时,加入的硝酸银和盐酸之间反应生成氯化银沉淀和硝酸,金属锌和硝酸反应不会产生氢气,影响氢气的量,故B错误;
C、在稀硫酸和铁粉反应制取氢气时,可以加入适量醋酸钠,醋酸钠可以和硫酸之间反应生成硫酸钠和醋酸,减慢反应速率,但是生成氢气的量不变,故C正确;
D、改用6 mL乙醇、4 mL浓H2SO4、4 mL冰醋酸后,各组分的物质的量浓度不变,所以不会影响反应速率,故D错误.
故选C.
B、盐酸和锌制取氢气时,加入的硝酸银和盐酸之间反应生成氯化银沉淀和硝酸,金属锌和硝酸反应不会产生氢气,影响氢气的量,故B错误;
C、在稀硫酸和铁粉反应制取氢气时,可以加入适量醋酸钠,醋酸钠可以和硫酸之间反应生成硫酸钠和醋酸,减慢反应速率,但是生成氢气的量不变,故C正确;
D、改用6 mL乙醇、4 mL浓H2SO4、4 mL冰醋酸后,各组分的物质的量浓度不变,所以不会影响反应速率,故D错误.
故选C.
点评:本题考查学生影响化学反应速率的因素知识,注意知识的归纳和梳理是解题的关键,属于综合知识的考查,难度不大.

练习册系列答案
 小学期末标准试卷系列答案
小学期末标准试卷系列答案
相关题目
用NA表示阿伏伽德罗常数,下列说法正确的是( )
| A、通常状况下,1NA个H2分子占有的体积是22.4L |
| B、1mol氧是32g |
| C、摩尔是国际七个基本物理量之一 |
| D、常温常压下,2.12gNa2CO3固体中含有的CO32-离子数位0.02NA |
下列说法正确的是( )
| A、在我们常用的元素周期表中,元素被划分为两类:金属元素和非金属元素 |
| B、在元素周期表中,每个纵列的价电子层的电子总数一定相等 |
| C、在元素周期表里,主族元素所在的族序数等于原子核外电子数 |
| D、在元素周期表中,s区,d区和ds区的元素都是金属元素 |
在一定体积的密闭容器中,进行如下的化学反应CO2(g)+H2(g)?CO(g)+H2O(g),其中
=K,K被称为化学平衡常数,其中K和温度的关系如下表:根据以上信息推断以下说法正确的是( )
| [CO]×[H20] |
| [CO2]×[H2] |
| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
| A、此反应为放热反应 |
| B、此反应只有达到平衡时,密闭容器中的压强才不会变化 |
| C、此反应达到1000℃时的反应速率比700℃时大 |
| D、该反应的化学平衡常数越大,反应物的转化率越低 |
某状况下,2gCO2 气体的体积是1120ml,2gA气体的体积是770ml,则A的相对分子质量为( )
| A、48 | B、64 | C、72 | D、56 |
 将锌片和铜片用导线相连后一同插入稀硫酸中,导线上便有电流通过.
将锌片和铜片用导线相连后一同插入稀硫酸中,导线上便有电流通过.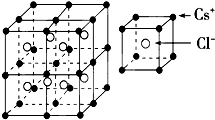 根据如图推测,CsCl晶体中两距离最近的Cs+间距离为a,则每个Cs+周围与其距离为a的Cs+数目为
根据如图推测,CsCl晶体中两距离最近的Cs+间距离为a,则每个Cs+周围与其距离为a的Cs+数目为