题目内容
 凯氏定氮法测定奶粉中蛋白质含量的步骤如下:
凯氏定氮法测定奶粉中蛋白质含量的步骤如下:①样品处理:准确称取奶粉试样1.000g置于烧瓶中,加入足量不含氮元素的试剂A,一定条件下充分反应,产物用水溶解并冷却后全部转移至100mL容量瓶中定容.
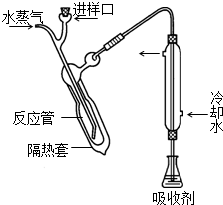
②碱化蒸馏:量取容量瓶中溶液10.00mL转移至如图所示的反应管中,再加入足量NaOH溶液,塞好进样口橡皮塞.通入高温水蒸气.用吸收剂吸收产生的气体.
③滴定:向吸收气体后的溶液中滴加2滴指示剂,用0.01mol/L HCl标准溶液滴定至终点.已知:
吸收剂中发生的反应为:NH3+4H3BO3═NH4HB4O7+5H2O;
滴定时发生的反应为:NH4HB4O7+HCl+5H2O═NH4Cl+4H3BO3.
根据以上知识回答下列问题:
1 样品处理的目的是
(2)冷凝管的作用是冷凝、导气、
(3)若蛋白质中氮元素的平均含量为16.0%,滴定终点时消耗盐酸标准液15.50mL,则该奶粉中蛋白质的含量为
(4)凯氏定氮法测定奶粉中蛋白质含量灵敏度高,操作简单,缺点是
考点:探究物质的组成或测量物质的含量
专题:实验探究和数据处理题
分析:凯氏定氮法测定奶粉中蛋白质含量原理为:通过样品处理把氮元素转化为NH4+,加入氢氧化钠转化为氨气,用吸收剂吸收转化为NH4HB4O7,用盐酸滴定,通过消耗盐酸的量来计算氮元素的含量和蛋白质的含量.
(1)从测量步骤可知样品处理目的是把蛋白质中氮元素转化为NH4+;氨水不稳定,温度高分解成氨气挥发,温度高可使反应中生成的氨气全部进入吸收液;
(2)根据氨气的性质考虑冷凝管的作用;
(3)根据滴定终点时消耗盐酸标准液15.50mL可计算出消耗盐酸的物质的量,盐酸的物质的量和氮元素的物质的量相等,设该奶粉中蛋白质的质量分数为x,则可以得出关系式:0.0155L×0.01mol/L×10×14g/mol=1.000g×16%×x,从而计算出此奶粉中蛋白质的质量分数;
(4)测定原理为:把蛋白质样品用强酸处理,使其中的氮元素释放出来,通过测定氮元素的质量从而换算出蛋白质的含量,此方法的局限性很明显,它把样品中释放出来的N元素全部归为蛋白质中的N元素,而样品中释放出来的N元素也可能不是从蛋白质中来的.
(1)从测量步骤可知样品处理目的是把蛋白质中氮元素转化为NH4+;氨水不稳定,温度高分解成氨气挥发,温度高可使反应中生成的氨气全部进入吸收液;
(2)根据氨气的性质考虑冷凝管的作用;
(3)根据滴定终点时消耗盐酸标准液15.50mL可计算出消耗盐酸的物质的量,盐酸的物质的量和氮元素的物质的量相等,设该奶粉中蛋白质的质量分数为x,则可以得出关系式:0.0155L×0.01mol/L×10×14g/mol=1.000g×16%×x,从而计算出此奶粉中蛋白质的质量分数;
(4)测定原理为:把蛋白质样品用强酸处理,使其中的氮元素释放出来,通过测定氮元素的质量从而换算出蛋白质的含量,此方法的局限性很明显,它把样品中释放出来的N元素全部归为蛋白质中的N元素,而样品中释放出来的N元素也可能不是从蛋白质中来的.
解答:
解:(1)从测量步骤可知样品处理目的是把蛋白质中氮元素转化为NH4+;氨水不稳定,温度高分解成氨气挥发,温度高可使反应中生成的氨气全部进入吸收液,
故答案为:将奶粉中氮元素全部转变为NH4+;使反应中生成的氨气全部进入吸收液;
(2)反应管中产生的氨气在冷凝管中冷凝后进入锥形瓶中被吸收,由于氨气极易溶于水,易倒吸,冷凝管容积大,不易倒吸,故冷凝管还有防倒吸作用,
故答案为:防止倒吸;
(3)通过样品处理把氮元素转化为NH4+,加入氢氧化钠转化为氨气,吸收剂中发生的反应为:NH3+4H3BO3═NH4HB4O7+5H2O;
滴定时发生的反应为:NH4HB4O7+HCl+5H2O═NH4Cl+4H3BO3,由此可找出关系式:
N~NH3~NH4HB4O7~HCl
14g 1mol
m 0.0155L×0.01mol/L
m=
=0.00217g,则1.000g样品中含N:0.0217g,设该奶粉中蛋白质的质量分数为x,则可以得出关系式:
0.0217g=1.000g×16%×x,解得x=0.136=13.6%;故答案为:13.6;
(4)测定原理为:把蛋白质样品用中的氮元素释放出来,通过测定氮元素的质量从而换算出蛋白质的含量,此方法的局限性很明显,它把样品中释放出来的N元素全部归为蛋白质中的N元素,若样品中含有其他含氮化合物,则无法准确测定蛋白质的含量,故答案为:无法确定氮元素是否一定来自于蛋白质.
故答案为:将奶粉中氮元素全部转变为NH4+;使反应中生成的氨气全部进入吸收液;
(2)反应管中产生的氨气在冷凝管中冷凝后进入锥形瓶中被吸收,由于氨气极易溶于水,易倒吸,冷凝管容积大,不易倒吸,故冷凝管还有防倒吸作用,
故答案为:防止倒吸;
(3)通过样品处理把氮元素转化为NH4+,加入氢氧化钠转化为氨气,吸收剂中发生的反应为:NH3+4H3BO3═NH4HB4O7+5H2O;
滴定时发生的反应为:NH4HB4O7+HCl+5H2O═NH4Cl+4H3BO3,由此可找出关系式:
N~NH3~NH4HB4O7~HCl
14g 1mol
m 0.0155L×0.01mol/L
m=
| 14g×0.0155L×0.01mol/L |
| 1mol |
0.0217g=1.000g×16%×x,解得x=0.136=13.6%;故答案为:13.6;
(4)测定原理为:把蛋白质样品用中的氮元素释放出来,通过测定氮元素的质量从而换算出蛋白质的含量,此方法的局限性很明显,它把样品中释放出来的N元素全部归为蛋白质中的N元素,若样品中含有其他含氮化合物,则无法准确测定蛋白质的含量,故答案为:无法确定氮元素是否一定来自于蛋白质.
点评:本题考查了蛋白质含量的测定,中等难度,利用关系式可简化计算,注意结合题给信息和装置图解题.

练习册系列答案
相关题目
用NA表示阿伏伽德罗常数,下列说法正确的是( )
| A、通常状况下,1NA个H2分子占有的体积是22.4L |
| B、1mol氧是32g |
| C、摩尔是国际七个基本物理量之一 |
| D、常温常压下,2.12gNa2CO3固体中含有的CO32-离子数位0.02NA |
某状况下,2gCO2 气体的体积是1120ml,2gA气体的体积是770ml,则A的相对分子质量为( )
| A、48 | B、64 | C、72 | D、56 |
下列说法错误的是( )
| A、淀粉溶液具有丁达尔效应 |
| B、有色玻璃不属于胶体 |
| C、明矾能净水 |
| D、瓯江水是浊液、胶体、溶液组成的混合体系 |
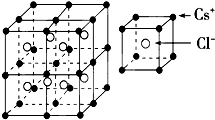 根据如图推测,CsCl晶体中两距离最近的Cs+间距离为a,则每个Cs+周围与其距离为a的Cs+数目为
根据如图推测,CsCl晶体中两距离最近的Cs+间距离为a,则每个Cs+周围与其距离为a的Cs+数目为