题目内容
15.设NA为阿伏伽德罗常数的值,下列说法正确的是( )| A. | 1molFeI2与1molCl2反应时转移的电子数为3NA | |
| B. | 2g H218O与D216O的混合物中所含中子、电子数目均为NA | |
| C. | 273K,101kPa下,28g乙烯与丙烯混合物中含有C-H键的数目为5NA | |
| D. | pH=1的H2SO4溶液10L,含H+的数目为2NA |
分析 A.1molFeI2与1molCl2反应时,氯气少量完全反应,依据氯气计算转移电子数;
B.H218O与D216O,摩尔质量、中子数、电子数都相等,1个H218O或者D216O含有中子数10,电子数10;
C.乙烯和丙烯分子中含有的碳氢键数目不同,由于不知二者的含量,无法计算含有的碳氢键数目;
D.根据PH=-lgc(H+)计算;
解答 解:A.1molFeI2与1molCl2反应,氯气完全反应生成2mol氯离子,转移的电子数为2NA,故A错误;
B.2g H218O与D216O的混合物物质的量为0.1mol,中所含中子、电子数目均为NA,故B正确;
C.由于乙烯和丙烯分子中含有的碳氢键数目不同,题中条件无法计算混合物中含有的碳氢键数目,故C错误;
D.pH=1H2SO4溶液PH=-lgc(H+)=1,H2SO4溶液c(H+)=0.1mol/L,10L溶液n(H+)=1mol,所含H+数目为NA,故D错误;
故选:B.
点评 本题考查了阿伏伽德罗常数的应用,明确物质的量与阿伏伽德罗常数、摩尔质量等物理量之间的转化关系为解答关键,注意有机物结构特点,题目难度中等.

练习册系列答案
相关题目
3.下列说法不正确的是( )
| A. | 126C和146C是一种核素 | |
| B. | 红磷和白磷互为同素异形体 | |
| C. | CH3COOCH2CH3和CH3CH2COOCH3是不同物质 | |
| D. | CH3CH2OH可看成是由-C2H5和-OH两种基团组成 |
10.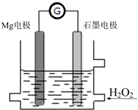 Mg-H2O2电池是一种化学电源,以Mg和石墨为电极,海水为电解质溶液,示意图如下.下列说法不正确的是( )
Mg-H2O2电池是一种化学电源,以Mg和石墨为电极,海水为电解质溶液,示意图如下.下列说法不正确的是( )
 Mg-H2O2电池是一种化学电源,以Mg和石墨为电极,海水为电解质溶液,示意图如下.下列说法不正确的是( )
Mg-H2O2电池是一种化学电源,以Mg和石墨为电极,海水为电解质溶液,示意图如下.下列说法不正确的是( )| A. | 石墨电极是该电池的正极 | |
| B. | 石墨电极上发生还原反应 | |
| C. | Mg电极的电极反应式:Mg-2e-=Mg2+ | |
| D. | 电池工作时,电子从Mg电极经导线流向石墨电极,再出石墨电极经电解质溶液流向Mg电极 |
7.下列说法不正确的是( )
| A. | 常温下,在0.10mol•L-1CH3COOH溶液中加入少量CH3COONa晶体,能使CH3COOH的电离度降低,溶液的pH增大 | |
| B. | 常温下向氯化铵溶液中加入少量氨水使溶液中c(NH4+)=c(Cl-),则混合液的pH=7 | |
| C. | 已知草酸氢钾溶液呈酸性,则在0.1 mol•L-1KHC2O4溶液中c(C2O42-)>c(K+)>c(H2C2O4) | |
| D. | pH=3的0.1 mol•L-1HA溶液与0.05 mol•L-1NaOH溶液等体积混合后所得溶液中:2c(H+)+c(HA)=c(A-)+2c(OH-) |
4.雌二醇的结构简式如图,下列说法不正确的是( )
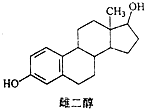

| A. | 能与Na、Na0H溶液、Na2CO3溶液反应 | |
| B. | 能发生加成反应、取代反应、消去反应 | |
| C. | 该分子中所有碳原子不可能在同一个平面内 | |
| D. | 可与FeC13溶液发生显色反应,但不能发生氧化反应 |
5.如图甲是一种利用微生物将废水中的尿素(H2NCONH2,氮元素显-3价)的化学能直接转化为电能,并生成对环境无害物质的装置,同时利用此装置的电能在铁上镀铜,下列说法中不正确的是( )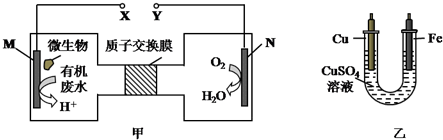

| A. | H十透过质子交换膜由左向右移动 | |
| B. | 铜电极应与Y相连接 | |
| C. | M电极反应式:H2NCONH2+H2O-6e-═CO2↑+N2↑+6H+ | |
| D. | 当N电极消耗0.25 mol气体时,则铁电极增重16g |