题目内容
9. 如图X为电源,椭圆形滤纸Y浸透饱和食盐水和酚酞试液,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色斑向c端扩散.下列判断正确的是( )
如图X为电源,椭圆形滤纸Y浸透饱和食盐水和酚酞试液,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色斑向c端扩散.下列判断正确的是( )| A. | b为电源的正极,d点周围变红 | B. | Cu电极质量减小,Pt电极质量增大 | ||
| C. | Z中溶液的pH先减小,后增大 | D. | 溶液中的SO42-向Pt电极定向移动 |
分析 有外接电源的装置是电解池,电解池放电时,连接电源正极的电极是阳极,连接电源负极的电极是阴极,电解质溶液中阴离子向阳极移动,阳离子向阴极移动,通电后Y中央的紫红色色斑向d端扩散,即带负电荷的高锰酸根向c端扩散,说明c是阳极,d是阴极,b是负极,a是正极,铜极是阳极,铂极为阴极.
通电时,阳极上铜失电子发生氧化反应,阴极上铜离子得电子发生还原反应,故在装置是个电镀装置,溶液中硫酸铜的浓度不变,根据阴阳极上析出的物质及溶液中离子浓度的变化判断正误.
解答 解:A、b为电源的负极,且通电时,饱和食盐水中氢离子得电子在d极上析出,导致d极附近氢氧根离子的浓度增大,溶液的碱性增强,所以滴有酚酞的试液会变红,故A错误;
B、通电时,铜作阳极,铂作阴极,铜极上铜失电子质量变小;铂极上铜离子得电子生成单质铜,所以铂极质量增大,故B正确;
C、通电时,铜作阳极,铂作阴极,铜极上铜失去电子从而铜溶解,铂极上铜离子得电子,故溶液硫酸铜溶液的浓度不变,则溶液中的pH值不变,故C错误;
D、通电时,电解池中阴离子向阳极移动,阳离子向阴极移动,即溶液中硫酸根离子向铜极移动,故D错误;
故选B.
点评 本题考查了电解池原理,明确高锰酸钾溶液中高锰酸根离子呈紫红色是解本题的关键,难度不大.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
4.钫(Fr)元素在周期表中位于第七周期,第IA族,根据钫在周期表中的位置推测其性质,其中错误的
是( )
是( )
| A. | 其单质的熔点比钠的熔点低 | B. | 其氧化物对应的水化物的碱性很强 | ||
| C. | 其原子半径在同一主族中是最大的 | D. | 在空气中燃烧只能生成Fr2O |
20.下列物质中,含有共价键的离子化合物的是( )
| A. | HCl | B. | MgCl2 | C. | NH4Cl | D. | NH3 |
17.下列关于有机化合物的说法正确的是( )
| A. | 2,2,7,7-四甲基辛烷的一氯取代物有4种 | |
| B. | 甲醇与分子式为C3H8O的某种有机物相差2个CH2原子团,故它们一定互为同系物 | |
| C. | 苯与浓硝酸、浓硫酸共热并保持50~60℃反应生成硝基苯 | |
| D. | 甲烷和 Cl2的反应与乙烯和 Br2的反应属于同一类型的反应 |
4.下列试剂中,标签上应标注如图标志的是( )


| A. | 汽油 | B. | 浓硫酸 | C. | 高锰酸钾 | D. | 酒精 |
14.汽车发动机中生成NO的反应为:N2(g)+O2(g)?2NO(g),t℃时,K=0.09.在t℃下甲、乙、丙三个恒容密闭容器中,投入N2(g) 和 O2(g) 模拟反应,起始浓度如表所示.下列判断不正确的是( )
| 起始浓度 | 甲 | 乙 | 丙 |
| c(N2)/mol•L-1 | 0.46 | 0.46 | 0.92 |
| c(O2)/mol•L-1 | 0.46 | 0.23 | 0.92 |
| A. | 起始时,反应速率:丙>甲>乙 | B. | 平衡时,c(NO):甲=丙>乙 | ||
| C. | 平衡时,N2的转化率:甲>乙 | D. | 平衡时,甲中c(N2)=0.4 mol•L-1 |
1.某同学为测定Na2CO3固体(含少量NaCl)的纯度,设计如图装置(含试剂)进行实验.
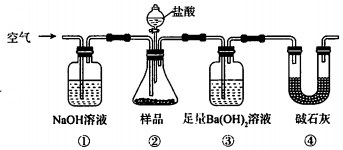
下列说法不正确的是( )

下列说法不正确的是( )
| A. | 必须在②③间添加吸收HCl的装置 | |
| B. | ④的作用是防止空气中的气体影响实验的精确度 | |
| C. | 通入空气的作用是保证②中产生的气体完全转移到③中 | |
| D. | 称取样品和③中产生的沉淀的质量即可求算Na2CO3固体的纯度 |
18.为确定下列置于空气中的物质是否变质,所选试剂(括号内的物质)不能达到目的是( )
| A. | 氯水(AgNO3溶液) | B. | NaOH溶液[Ba(OH)2溶液] | ||
| C. | FeSO4溶液(KSCN溶液) | D. | KI溶液(淀粉溶液) |
19.将少量的铝投入过量的氢氧化钠溶液中充分反应,下列有关所得混合溶液的叙述正确的是( )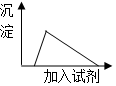

| A. | 该溶液中,Ag+、K+、NH4+、SO42-可以大量共存 | |
| B. | 该溶液中,Na+、OH-、NO3-、CO32-不能大量共存 | |
| C. | 向该溶液中逐滴加入AlCl3溶液,生成沉淀与加入AlCl3溶液关系如图 | |
| D. | 向该溶液中逐滴加入稀盐酸,生成沉淀与加入稀盐酸关系如图 |