题目内容
下列关于Fe(OH)3胶体的制备方法,正确的是( )
A、.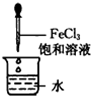 |
B、.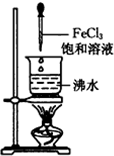 |
C、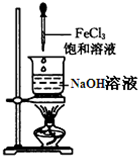 |
D、.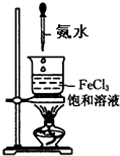 |
考点:胶体的重要性质
专题:溶液和胶体专题
分析:实验室制备氢氧化铁胶体是在沸腾的蒸馏水中加入饱和的氯化铁溶液,注意不能用玻璃棒搅拌、当液体变成红褐色时立即停止加热,以此解答.
解答:
解:A.反应过程需要加热到沸腾,故A错误;
B.实验室制备氢氧化铁胶体是在沸腾的蒸馏水中加入饱和的氯化铁溶液,故B正确;
C.氯化铁与氢氧化钠发生反应:FeCl3+3NaOH=Fe(OH)3↓+3NaCl,得不到氢氧化铁胶体,故C错误;
D.氨水与氯化铁发生反应:Fe3++3NH3.H2O=Fe(OH)3↓+3NH4+,得不到氢氧化铁胶体,故D错误;
故选:B.
B.实验室制备氢氧化铁胶体是在沸腾的蒸馏水中加入饱和的氯化铁溶液,故B正确;
C.氯化铁与氢氧化钠发生反应:FeCl3+3NaOH=Fe(OH)3↓+3NaCl,得不到氢氧化铁胶体,故C错误;
D.氨水与氯化铁发生反应:Fe3++3NH3.H2O=Fe(OH)3↓+3NH4+,得不到氢氧化铁胶体,故D错误;
故选:B.
点评:本题考查了氢氧化铁胶体的制备,题目难度不大,注意制备氢氧化铁胶体时为防止产生的胶体发生聚沉,加热到溶液呈现透明的红褐色为止,制备过程中不能用玻璃棒搅拌,加入的氯化铁溶液不能过量.

练习册系列答案
相关题目
在强酸性和强碱性溶液中均不能大量共存的离子组是( )
| A、K+、Fe3+、SO42-、NO3- |
| B、K+、Na+、CO32-、OH- |
| C、Ca2+、Na+、NO3-、Cl- |
| D、Na+、Mg2+、CH3COO-、Cl- |
自然界中氧元素有三种同位素16O、17O、18O,氧元素的相对原子质量为15.9994,由此可知16O的相对原子质量为( )
| A、>16 | B、<16 |
| C、=16 | D、不能确定 |
下列离子反应方程式,书写正确的是( )
| A、用小苏打(碳酸氢钠)治疗胃酸过多:HCO3-+H+=CO2↑+H2O |
| B、向稀盐酸中投入银粉2Ag+2H+=2Ag++H2↑ |
| C、在澄清石灰水中通入过量的CO2:Ca2++2OH-+CO2=CaCO3↓+H2O |
| D、饱和FeCl3溶液滴入沸水中制备氢氧化铁胶体:Fe3++3H2O=Fe(OH)3↓+3H+ |
下列反应中,属于加成反应的是( )
A、CH3Cl+Cl2
| |||
B、CH2=CH2+H2O
| |||
C、2CH3CH2OH+O2
| |||
D、 |
某单烯烃与H2 发生加成反应后得到的产物的结构简式如下:(CH3)2CH-CH2-C(CH3)3这种烯烃的结构式可能有几种( )
| A、3种 | B、5种 | C、6种 | D、7种 |
一定条件下,可逆反应N2+3H2?2NH3达到化学平衡状态,下列说法一定正确的是( )
| A、每1molN≡N断裂的同时有2 mol N-H生成 | ||
| B、N2、H2、NH3的浓度之比为1:3:2 | ||
| C、N2减少的速率和NH3减少的速率之比为1:2 | ||
D、气体体积为初始体积的
|