题目内容
(1)设NA为阿伏加德罗常数的数值,如果a g某气体中含有的分子数为b,则c g某气体在标准状况下的体积约是 (用含NA的式子表示).
(2)把V L含有MgSO4与K2SO4的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为Mg(OH)2;另一份加入含b mol BaCl2的溶液,恰好使SO
完全沉淀为BaSO4,则原混合溶液中钾离子的物质的量浓度为 .
(2)把V L含有MgSO4与K2SO4的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为Mg(OH)2;另一份加入含b mol BaCl2的溶液,恰好使SO
2- 4 |
考点:离子方程式的有关计算,物质的量的相关计算
专题:计算题
分析:(1)同种气体,其质量与分子数成正比,然后根据n=
、V=n×Vm来计算;
(2)混合溶液分成两等份,每份溶液浓度相同.一份加入含a mol NaOH的溶液,恰好使镁离子完全转化为Mg(OH)2,可知该份中n(Mg2+)=n[Mg(OH)2]=
n(NaOH);另一份加入含bmol BaCl2的溶液,恰好使硫酸根离子完全沉淀为BaSO4,根据钡离子与硫酸根守恒可知该份中n(SO42-)=n(BaSO4)=n(BaCl2),再利用电荷守恒可知每份中2n(Mg2+)+n(K+)=2(SO42-),据此计算每份中n(K+),根据c=
计算钾离子的浓度.
| N |
| NA |
(2)混合溶液分成两等份,每份溶液浓度相同.一份加入含a mol NaOH的溶液,恰好使镁离子完全转化为Mg(OH)2,可知该份中n(Mg2+)=n[Mg(OH)2]=
| 1 |
| 2 |
| n |
| V |
解答:
解:(1)解:a克某气体中含有的分子数为b,则c克气体含有的分子数为
,
c克该气体的物质的量为
=
mol,
在标准状况下Vm=22.4L/mol,则体积为
mol×22.4L/mol=
L,故答案为:
L;
(2)混合溶液分成两等份,每份溶液浓度与原溶液浓度相同.一份加入含a mol NaOH的溶液,恰好使镁离子完全转化为Mg(OH)2,可知该份中n(Mg2+)=n[Mg(OH)2]=
n(NaOH)=
mol;
另一份加入含bmol BaCl2的溶液,恰好使硫酸根离子完全沉淀为BaSO4,根据钡离子与硫酸根守恒可知该份中n(SO42-)=n(BaSO4)=n(BaCl2)=bmol,
每份溶液中2n(Mg2+)+n(K+)=2(SO42-),故每份溶液中n(K+)=2×bmol-2×
mol=(2b-a)mol,
故每份溶液中钾离子的浓度=
=
mol/L,即原溶液中钾离子的浓度为
mol/L,
故答案为:
mol/L.
| cb |
| a |
c克该气体的物质的量为
| ||
| NA |
| bc |
| aNA |
在标准状况下Vm=22.4L/mol,则体积为
| bc |
| aNA |
| 22.4bc |
| a?NA |
| 22.4bc |
| a?NA |
(2)混合溶液分成两等份,每份溶液浓度与原溶液浓度相同.一份加入含a mol NaOH的溶液,恰好使镁离子完全转化为Mg(OH)2,可知该份中n(Mg2+)=n[Mg(OH)2]=
| 1 |
| 2 |
| a |
| 2 |
另一份加入含bmol BaCl2的溶液,恰好使硫酸根离子完全沉淀为BaSO4,根据钡离子与硫酸根守恒可知该份中n(SO42-)=n(BaSO4)=n(BaCl2)=bmol,
每份溶液中2n(Mg2+)+n(K+)=2(SO42-),故每份溶液中n(K+)=2×bmol-2×
| a |
| 2 |
故每份溶液中钾离子的浓度=
| (2b-a)mol | ||
|
| 2(2b-a) |
| V |
| 2(2b-a) |
| V |
故答案为:
| 2(2b-a) |
| V |
点评:本题考查离子反应的有关混合计算,为高频考点,题目难度中等,根据电荷守恒计算钾离子的物质的量是关键,侧重分析能力及计算能力的考查.

练习册系列答案
相关题目
下列关于Fe(OH)3胶体的制备方法,正确的是( )
A、.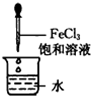 |
B、.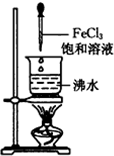 |
C、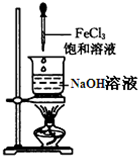 |
D、.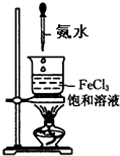 |
原子序数小于18的元素X,其原子最外层中未成对电子数最多,含这种元素的阴离子可能是( )
| A、XO3- |
| B、XO32- |
| C、XO42- |
| D、XO4- |
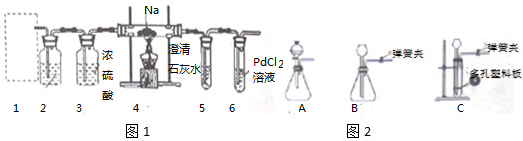
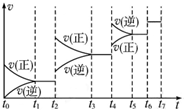 煤化工是以煤为原料,经过加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程.
煤化工是以煤为原料,经过加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程.