题目内容
某单烯烃与H2 发生加成反应后得到的产物的结构简式如下:(CH3)2CH-CH2-C(CH3)3这种烯烃的结构式可能有几种( )
| A、3种 | B、5种 | C、6种 | D、7种 |
考点:同分异构现象和同分异构体
专题:同系物和同分异构体
分析:加成反应指有机物分子中的不饱和键断裂,断键原子与其他原子或原子团相结合,生成新的化合物的反应.根据加成原理采取逆推法还原C=C双键,烷烃分子中相邻碳原子上均带氢原子的碳原子间是对应烯烃存在碳碳双键的位置.还原双键时注意:先判断该烃结构是否对称,如果对称,只考虑该分子一边的结构和对称线两边相邻碳原子即可;如果不对称,要全部考虑,然后各去掉相邻碳原子上的一个氢原子形成双键.
解答:
解:根据烯烃与H2加成反应的原理,推知该烷烃分子中相邻碳原子上均带氢原子的碳原子间是对应烯烃存在碳碳双键的位置,因此相应烯烃分子中存在碳碳双键的位置有3种, (标号处为碳碳双键的位置).
(标号处为碳碳双键的位置).
故选A.
 (标号处为碳碳双键的位置).
(标号处为碳碳双键的位置).故选A.
点评:本题以加成反应为载体,考查同分异构体的书写,理解加成反应原理是解题的关键,采取逆推法还原C=C双键,注意分析分子结构是否对称,防止重写、漏写.

练习册系列答案
 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案 导学与测试系列答案
导学与测试系列答案
相关题目
下列关于Fe(OH)3胶体的制备方法,正确的是( )
A、.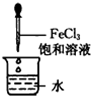 |
B、.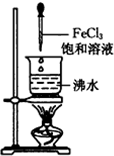 |
C、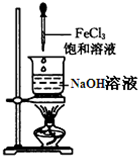 |
D、.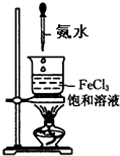 |
用四氯化碳萃取碘的饱和水溶液中的碘,下列说法中不正确的是( )
| A、实验使用的主要仪器是分液漏斗 |
| B、碘的四氯化碳溶液呈紫红色 |
| C、分液时,水从分液漏斗下口流出,碘的四氯化碳溶液从漏斗上口倒出 |
| D、碘在四氯化碳中的溶解度比在水中溶解度大 |
已知热化学方程式:①CO(g)+
O2 (g)=CO2 (g)△H=-283.0kJ?mol-1②H2(g)+
O2(g)=H2O(g);△H=-241.8kJ?mol-1则下列说法正确的是( )

| 1 |
| 2 |
| 1 |
| 2 |

| A、H2的燃烧热为241.8kJ?mol-1 |
| B、根据②推知反应H2(g)+O2 (g)=H2O(l);△H>-241.8kJ?mol-1 |
| C、H2(g)转变成H2O(g)的化学反应一定要释放能量 |
| D、由反应①、②可知如图所示的热化学方程式为CO(g)+H2O(g)=CO2(g)+H2(g)△H=-41.2kJ?mol-1 |
甲醛、乙醛,丙醛的混合物中,测得H的质量分数为9%,则混合物中O的质量分数( )
| A、37% | B、16% |
| C、6.6% | D、无法确定 |
原子序数小于18的元素X,其原子最外层中未成对电子数最多,含这种元素的阴离子可能是( )
| A、XO3- |
| B、XO32- |
| C、XO42- |
| D、XO4- |
下列说法正确的是( )
| A、铜锌原电池工作时,若有6.5g锌被溶解,电路中就有0.1mol电子通过 |
| B、原电池装置中,电子从正极流向负极 |
| C、可利用CH4和O2的反应设计成原电池 |
| D、在周期表中金属和非金属的分界处易寻找到催化剂和耐高温、耐腐蚀的合金材料 |
设NA为阿佛加德罗常数,下列说法不正确的是( )
| A、18g水中含有的电子数为10NA |
| B、标准状态下,22.4L氦气中含NA个氦原子 |
| C、1molCl2与金属Na完全反应,可以得到2NA个电子 |
| D、在2mol/L的硝酸镁溶液中含有的硝酸根离子数位4NA |