题目内容
下列离子反应方程式,书写正确的是( )
| A、用小苏打(碳酸氢钠)治疗胃酸过多:HCO3-+H+=CO2↑+H2O |
| B、向稀盐酸中投入银粉2Ag+2H+=2Ag++H2↑ |
| C、在澄清石灰水中通入过量的CO2:Ca2++2OH-+CO2=CaCO3↓+H2O |
| D、饱和FeCl3溶液滴入沸水中制备氢氧化铁胶体:Fe3++3H2O=Fe(OH)3↓+3H+ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.反应生成氯化钠、水、二氧化碳;
B.Ag与稀盐酸不反应;
C.通入过量的CO2反应生成碳酸氢钙;
D.生成胶体,不是沉淀.
B.Ag与稀盐酸不反应;
C.通入过量的CO2反应生成碳酸氢钙;
D.生成胶体,不是沉淀.
解答:
解:A.用小苏打(碳酸氢钠)治疗胃酸过多的离子反应为HCO3-+H+=CO2↑+H2O,故A正确;
B.向稀盐酸中投入银粉,不反应,不能写离子反应,故B错误;
C.在澄清石灰水中通入过量的CO2的离子反应为OH-+CO2=HCO3-,故C错误;
D.饱和FeCl3溶液滴入沸水中制备氢氧化铁胶体的离子反应为Fe3++3H2O
Fe(OH)3(胶体)+3H+,故D错误;
故选A.
B.向稀盐酸中投入银粉,不反应,不能写离子反应,故B错误;
C.在澄清石灰水中通入过量的CO2的离子反应为OH-+CO2=HCO3-,故C错误;
D.饱和FeCl3溶液滴入沸水中制备氢氧化铁胶体的离子反应为Fe3++3H2O
| ||
故选A.
点评:本题考查离子反应书写的正误判断,为高频考点,把握发生的化学反应及离子反应的书写方法为解答的关键,涉及与量有关的离子反应、水解反应等,综合性较强,题目难度不大.

练习册系列答案
相关题目
下列溶液中,跟100mL 0.15mol/LNa2SO4溶液所含的SO42-物质的量浓度相同的是( )
| A、200 mL 0.15 mol/L MgSO4 溶液 |
| B、50 mL 0.05 mol/L Al2(SO4)3溶液 |
| C、150 mL 1 mol/L Na2SO4 溶液 |
| D、300 mL 0.5 mol/L CuSO4 溶液 |
下列关于Fe(OH)3胶体的制备方法,正确的是( )
A、.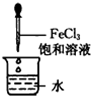 |
B、.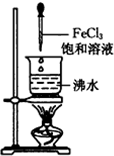 |
C、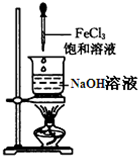 |
D、.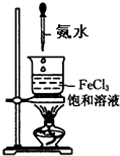 |
下列化学反应的离子方程式正确的是( )
| A、澄清石灰水中通入过量二氧化碳Ca2++CO2+2OH-═CaCO3↓+H2O | ||
B、氢氧化钡溶液与稀硫酸反应:Ba2++OH-+H++SO
| ||
| C、氢氧化铜加到稀盐酸中:Cu(OH)2+2H+═Cu2++2H2O | ||
| D、向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O═Fe(OH)3↓+3H+ |
用四氯化碳萃取碘的饱和水溶液中的碘,下列说法中不正确的是( )
| A、实验使用的主要仪器是分液漏斗 |
| B、碘的四氯化碳溶液呈紫红色 |
| C、分液时,水从分液漏斗下口流出,碘的四氯化碳溶液从漏斗上口倒出 |
| D、碘在四氯化碳中的溶解度比在水中溶解度大 |
甲醛、乙醛,丙醛的混合物中,测得H的质量分数为9%,则混合物中O的质量分数( )
| A、37% | B、16% |
| C、6.6% | D、无法确定 |
以下说法正确的是( )
| A、强电解质的水溶液导电性不一定比弱电解质的水溶液导电性强 |
| B、较多的金属钠着火可用泡沫灭火器灭火 |
| C、少量的金属钠可保存在CCl4中 |
| D、由于Na2O与水反应生成NaOH而导电,所以NaOH是电解质,Na2O是非电解质 |
 煤化工是以煤为原料,经过加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程.
煤化工是以煤为原料,经过加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程.