题目内容
自然界中氧元素有三种同位素16O、17O、18O,氧元素的相对原子质量为15.9994,由此可知16O的相对原子质量为( )
| A、>16 | B、<16 |
| C、=16 | D、不能确定 |
考点:同位素及其应用
专题:原子组成与结构专题
分析:元素相对原子质量=各种同位素的丰度与质量数的乘积之和,据此解题.
解答:
解:元素相对原子质量=各种同位素的丰度与质量数的乘积之和.氧元素的相对原子质量为15.9994,16O的原子量最小,应小于15.9994.
故选B.
故选B.
点评:本题考查平均相对原子质量的计算,比较基础,侧重对基础知识的巩固,注意对基础知识的理解掌握.

练习册系列答案
相关题目
下列化学用语的理解正确的是( )
A、2-丁醇的结构简式: |
B、电子式 :可以表示羟基,也可以表示氢氧根离子 :可以表示羟基,也可以表示氢氧根离子 |
C、比例模型  :可以表示甲烷分子,也可以表示四氯化碳分子 :可以表示甲烷分子,也可以表示四氯化碳分子 |
D、聚丙烯的结构简式: |
下列关于Fe(OH)3胶体的制备方法,正确的是( )
A、.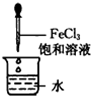 |
B、.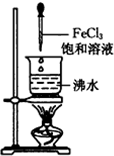 |
C、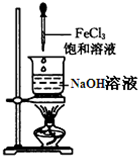 |
D、.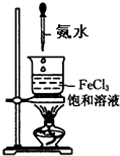 |
黑火药爆炸时发生:S+2KNO3+3C=K2S+N2↑+3CO2↑,其中被还原的物质是( )
| A、S和KNO3 |
| B、C 和S |
| C、KNO3 |
| D、C 和KNO3 |
已知热化学方程式:①CO(g)+
O2 (g)=CO2 (g)△H=-283.0kJ?mol-1②H2(g)+
O2(g)=H2O(g);△H=-241.8kJ?mol-1则下列说法正确的是( )

| 1 |
| 2 |
| 1 |
| 2 |

| A、H2的燃烧热为241.8kJ?mol-1 |
| B、根据②推知反应H2(g)+O2 (g)=H2O(l);△H>-241.8kJ?mol-1 |
| C、H2(g)转变成H2O(g)的化学反应一定要释放能量 |
| D、由反应①、②可知如图所示的热化学方程式为CO(g)+H2O(g)=CO2(g)+H2(g)△H=-41.2kJ?mol-1 |
萤火虫发光原理如下:

关于荧光素及氧化荧光素的叙述,正确的是( )

关于荧光素及氧化荧光素的叙述,正确的是( )
| A、互为同系物 |
| B、均可发生硝化反应 |
| C、均最多有7个碳原子共平面 |
| D、均可使FeCl3溶液变紫色 |