题目内容
13.下列说法错误的是( )| A. | 反应产物的总焓与反应物的总焓之差,称为反应焓变 | |
| B. | 反应产物的总焓小于反应物的总焓,该反应为吸热反应 | |
| C. | 同一反应在不同温度下进行,其焓变是不同的 | |
| D. | 已知2NO2(g)═N2O4(g)△H1,N2O4(g)═2NO2(g)△H2,则△H1=-△H2 |
分析 焓变为反应产物的总焓与反应物的总焓之差,当反应产物的总焓小于反应物的总焓,为放热反应,否则为吸热反应,温度不同,焓变不同,可逆反应的焓变绝对值相同,以此解答该题.
解答 解:A.焓为物质的总能量,焓变等于反应产物的总焓与反应物的总焓之差,故A正确;
B.反应产物的总焓小于反应物的总焓,则△H<0,为放热反应,故B错误;
C.温度不同,物质的焓不同,则焓变不同,故C正确;
D.可逆反应的焓变绝对值相同,但数值相反,故D正确.
故选B.
点评 本题是对化学变化与能量的考查,主要考查学生的分析能力和基本理论的运用的考查,注意相关概念的理解,题目难度不大.

练习册系列答案
相关题目
3.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 常温常压下的33.6 L氯气与27 g铝充分反应,转移的电子数为3NA | |
| B. | 标准状况下,0.5 NA 个NO和0.5 NA 个O2混合气体的体积约为22.4 L | |
| C. | 一定条件下,将1 mol N2与3 mol H2混合反应后,生成NH3分子的数目为2NA | |
| D. | 在电解CuSO4溶液的实验中,测得电解后溶液pH=0,又知电解后溶液体积为1 L,在阳极析出的气体分子数约为0.25NA |
4.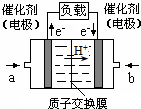 可给笔记本电脑供电的甲醇燃料电池已经面世,其结构示意图如下.甲醇在催化剂作用下提供质子(H+)和电子.电子经外电路、质子经内电路到达另一极与氧气反应.该电池总反应式为:2CH3OH+3O2═2CO2+4H2O.下列说法中正确的是( )
可给笔记本电脑供电的甲醇燃料电池已经面世,其结构示意图如下.甲醇在催化剂作用下提供质子(H+)和电子.电子经外电路、质子经内电路到达另一极与氧气反应.该电池总反应式为:2CH3OH+3O2═2CO2+4H2O.下列说法中正确的是( )
 可给笔记本电脑供电的甲醇燃料电池已经面世,其结构示意图如下.甲醇在催化剂作用下提供质子(H+)和电子.电子经外电路、质子经内电路到达另一极与氧气反应.该电池总反应式为:2CH3OH+3O2═2CO2+4H2O.下列说法中正确的是( )
可给笔记本电脑供电的甲醇燃料电池已经面世,其结构示意图如下.甲醇在催化剂作用下提供质子(H+)和电子.电子经外电路、质子经内电路到达另一极与氧气反应.该电池总反应式为:2CH3OH+3O2═2CO2+4H2O.下列说法中正确的是( )| A. | 右边的电极为电池的负极,b处通入的是空气 | |
| B. | 左边的电极为电池的负极,a处通入的是甲醇 | |
| C. | 电池负极的反应式为:CH3OH+H2O═CO2+6H++4e- | |
| D. | 电池正极的反应式为:O2+2H2O+4e-═4OH- |
1.下列说法正确的是( )
| A. | 水的离子积常数KW随着温度的升高而增大,说明水的电离过程是吸热的 | |
| B. | 弱电解质溶液稀释后,溶液中各种离子浓度一定都减小 | |
| C. | 某盐的水溶液呈酸性,该盐一定是强酸弱碱盐 | |
| D. | 中和相同体积相同pH的盐酸和醋酸溶液所需NaOH的物质的量相同 |
8.下列说法正确的是( )
| A. | 据Ksp(AgCl)=1.77×10-10,Ksp(Ag2CrO4)=2.0×10-12,可推知AgCl溶解度比Ag2CrO4的溶解度大 | |
| B. | 0.1mol/L的ZnCl2溶液中通入足量硫化氢最终得不到ZnS沉淀是因为c(Zn2+)•c(S2-)<Ksp(ZnS) | |
| C. | 向碳酸钡沉淀中加入稀硫酸,沉淀发生转化,可推知硫酸钡的Ksp比碳酸钡的大 | |
| D. | AgCl在10 mL 0.1 mol/L的KCl中溶解的质量比在10 mL 0.05 mol/L的AgNO3溶液中少 |
18.将浓度为0.1mol•L-1CH3COOH溶液加水不断稀释,下列各量始终保持增大的是( )
| A. | c(H+) | B. | $\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ | C. | $\frac{c(C{H}_{3}CO{O}^{-})}{c({H}^{+})}$ | D. | Ka(CH3COOH) |
2.下列微粒中,对水的电离平衡不产生影响的是( )
| A. | 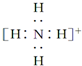 | B. | 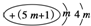 | C. | 26R3+ | D. | 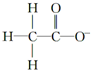 |
3.如图是氢氧燃料电池构造示意图.关于该电池的说法不正确的是( )


| A. | a极是正极 | B. | 电池总反应式为:2H2+O2=2H2O | ||
| C. | 电子由b通过灯泡流向a | D. | 氢氧燃料电池是环保电池 |