题目内容
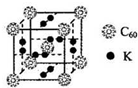
1.(1)氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料.已知 金刚石中的C-C的键长为154.45pm,C60中C一C键长为145〜140pm,有同学据此认为C60的熔点高于金刚石,你认为此说法是否正确不正确,C60是分子晶体,熔化时破坏的是分子间作用力,无需破坏共价键,而分子间作用力较弱,所以能量较低,所以C60熔点低于金刚石 (填“正确”或“不正确”),并阐述理由.(2)科学家把C60和钾掺杂在一起制造了一种富勒烯化合物,其晶胞如图所示,该物质在低温时是一种超导体.写出基态钾原子的价电子排布式4s1,该物质中K原子和C60分子的个数比为3:1.
(3)继C60后,科学家又合成了Si60、N60,C、Si、N原子.电负性由大到小的顺序是N>C>Si,NCl3分子的价层电子对互斥理论模型为正四面体.Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足 8电子稳定结构,则分子中π键的数目为30.
分析 (1)物质的熔点与晶体类型有关,原子晶体的熔点大于分子晶体;
(2)K是19号元素,其原子核外有19个电子,4s电子为其价电子,且4s能级上只有一个电子;根据均摊法计算该晶胞中K原子和C60个数,从而确定化学式;
(3)同一周期元素,元素电负性随着原子序数增大而增大,同一主族元素其电负性随着原子序数增大而减弱;
NCl3分子中N原子价层电子对个数是4且含有一个孤电子对,据此判断该分子VSEPR模型;
Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,所以每个硅原子和其中两个硅原子形成共价单键,和另外的一个硅原子形成共价双键,据此计算分子中π键的数目.
解答 解:(1)原子晶体的熔点大于分子晶体,金刚石是原子晶体,C60是分子晶体,C60是分子晶体,熔化时破坏的是分子间作用力,无需破坏共价键,而分子间作用力较弱,所以能量较低,所以C60熔点低于金刚石,故答案为:不正确,因为金刚石是原子晶体,而C60是分子晶体;
(2)K是19号元素,其原子核外有19个电子,4s电子为其价电子,且4s能级上只有一个电子,所以其价电子排布式为4s1;
该晶胞中K原子个数=12×$\frac{1}{2}$=6,C60个数=1+8×$\frac{1}{8}$=2,所以K原子和C60个数之比=6:2=3:1,
故答案为:4s1;3:1;
(3)同一周期元素,元素电负性随着原子序数增大而增大,同一主族元素其电负性随着原子序数增大而减弱,所以电负性大小顺序是N>C>Si;
NCl3分子中N原子价层电子对个数是4且含有一个孤电子对,据此判断该分子VSEPR模型为正四面体;
Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,所以每个硅原子和其中两个硅原子形成共价单键,和另外的一个硅原子形成共价双键,所以平均每个Si60形成π键数目为:60×$\frac{1}{2}$=30,
故答案为:N>C>Si;正四面体;30.
点评 本题考查物质结构和性质,为高频考点,涉及晶胞计算、电负性大小比较、原子核外电子排布、分子空间构型判断等知识点,侧重考查学生分析判断、空间想象、计算能力,难点是晶胞计算.

 口算能手系列答案
口算能手系列答案| A. | 焚烧秸秆,还肥于田 | B. | 净化废水,循环利用 | ||
| C. | 低碳出行,植树造林 | D. | 开发风能,利用地热 |
| A. | 硫酸的摩尔质量是98 g | B. | 18 g水中含有水分子数为NA | ||
| C. | O2的摩尔质量等于其相对分子质量 | D. | 1 mol CO的质量为28 g•mol-1 |
| A. | K2SO4、HNO3、BaCl2 | B. | NaOH、NH4Cl、Mg(NO3)2 | ||
| C. | NH4HCO3、KCl、NaCl | D. | KMnO4、NaCl、H2SO4 |
 氧化铁可溶于稀盐酸.某同学想知道是稀盐酸中的哪种粒子(H2O、H+、Cl-)能使氧化铁溶解.设计如下实验:
氧化铁可溶于稀盐酸.某同学想知道是稀盐酸中的哪种粒子(H2O、H+、Cl-)能使氧化铁溶解.设计如下实验: