题目内容
10.将下列各组物质溶于水后,得到无色溶液的一组是( )| A. | K2SO4、HNO3、BaCl2 | B. | NaOH、NH4Cl、Mg(NO3)2 | ||
| C. | NH4HCO3、KCl、NaCl | D. | KMnO4、NaCl、H2SO4 |
分析 根据离子之间不能结合生成沉淀、气体、水等,不能发生氧化还原反应等,则物质大量共存,并结合离子的颜色来解答.
解答 解:A.K2SO4、BaCl2反应生成硫酸钡沉淀,不能大量共存,故A错误;
B.NaOH、NH4Cl反应生成一水合氨,NaOH、Mg(NO3)2反应生成氢氧化镁沉淀,不能大量共存,故B错误;
C.该组物质自己不反应,可大量共存,且溶于水均为无色,故C正确;
D.KMnO4、NaCl、H2SO4发生氧化还原反应生成氯气,且KMnO4为紫色,与无色不符,故D错误;
故选C.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应、氧化还原反应的离子共存考查,题目难度不大.

练习册系列答案
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案
相关题目
20.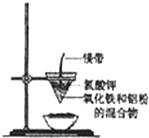 研究性学习小组的同学们用如图所示装置进行铝热反应的实验,请回答:
研究性学习小组的同学们用如图所示装置进行铝热反应的实验,请回答:
(1)氧化铁与铝反应的化学方程式是2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3,
(2)镁带的作用是燃烧时提供热量,引发反应;氯酸钾的作用是受热分解提供氧气,帮助镁条燃烧.
(3)同学们在实验过程中观察到纸漏斗的下部被烧穿,有熔融物落入沙中.他们为探究此熔融物的成分,查阅(化学手册)得知有关物质的熔点、沸点数据如下:
同学们分析数据后推测该熔融物是一种合金,其中的金属是Al、Fe,溶解该合金可选用下列试剂中的BC(填序号).
A.FeSO4溶液 B.稀硫酸 C.稀硝酸 D.NaOH溶液.
 研究性学习小组的同学们用如图所示装置进行铝热反应的实验,请回答:
研究性学习小组的同学们用如图所示装置进行铝热反应的实验,请回答:(1)氧化铁与铝反应的化学方程式是2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3,
(2)镁带的作用是燃烧时提供热量,引发反应;氯酸钾的作用是受热分解提供氧气,帮助镁条燃烧.
(3)同学们在实验过程中观察到纸漏斗的下部被烧穿,有熔融物落入沙中.他们为探究此熔融物的成分,查阅(化学手册)得知有关物质的熔点、沸点数据如下:
| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1462 |
| 沸点/℃ | 2467 | 2980 | 2750 | - |
A.FeSO4溶液 B.稀硫酸 C.稀硝酸 D.NaOH溶液.
18.下列各组含氯元素的物质中,氯元素化合价相同的一组是( )
| A. | Cl2 HCl | B. | ClO2 NaClO2 | C. | NaCl HClO | D. | KClO3 Ca(ClO3)2 |
5.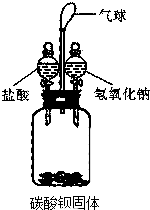 某研究性学习小组用如图所示装置进行如下实验(不考虑气体与水或盐的反应)
某研究性学习小组用如图所示装置进行如下实验(不考虑气体与水或盐的反应)
(1)先向广口瓶中加入一定量盐酸溶液至固体恰好全部溶解为止,关闭活塞,振荡,观察到气球变大.然后再将一定量氢氧化钠溶液加入广口瓶中,关闭活塞,振荡,发现气球明显变小,请写出引起气球变小的化学反应方程式2NaOH+CO2=Na2CO3+H2O,同时在广口瓶中还能观察到的现象是产生白色沉淀.
(2)实验结束后,同学们对广口瓶中的溶液进行探究.
提出问题:广口瓶中的溶液含有哪些溶质?
交流讨论:经过大家对广口瓶中所发生的反应进行分析,认为瓶内一定含有的一种溶质是(填化学式,下同)NaCl.小明取广口瓶内溶液少量于试管中,向其中加入过量稀盐酸,发现有气泡产生.由此得出结论:广口瓶溶液中还含有的溶质是Na2CO3.小红认为,可能还存在BaCl2,大家一致认为小红的结论是错误的,理由是BaCl2和Na2CO3在溶液中不共存.后经大家讨论,达成共识:广口瓶溶液中还可能存在NaOH.
实验设计:
考虑到已经确定的两种溶质中有一种溶质的存在对氢氧化钠的检验造成干扰,设计方案先将它除去后再检验.具体步骤如表:
 某研究性学习小组用如图所示装置进行如下实验(不考虑气体与水或盐的反应)
某研究性学习小组用如图所示装置进行如下实验(不考虑气体与水或盐的反应)(1)先向广口瓶中加入一定量盐酸溶液至固体恰好全部溶解为止,关闭活塞,振荡,观察到气球变大.然后再将一定量氢氧化钠溶液加入广口瓶中,关闭活塞,振荡,发现气球明显变小,请写出引起气球变小的化学反应方程式2NaOH+CO2=Na2CO3+H2O,同时在广口瓶中还能观察到的现象是产生白色沉淀.
(2)实验结束后,同学们对广口瓶中的溶液进行探究.
提出问题:广口瓶中的溶液含有哪些溶质?
交流讨论:经过大家对广口瓶中所发生的反应进行分析,认为瓶内一定含有的一种溶质是(填化学式,下同)NaCl.小明取广口瓶内溶液少量于试管中,向其中加入过量稀盐酸,发现有气泡产生.由此得出结论:广口瓶溶液中还含有的溶质是Na2CO3.小红认为,可能还存在BaCl2,大家一致认为小红的结论是错误的,理由是BaCl2和Na2CO3在溶液中不共存.后经大家讨论,达成共识:广口瓶溶液中还可能存在NaOH.
实验设计:
考虑到已经确定的两种溶质中有一种溶质的存在对氢氧化钠的检验造成干扰,设计方案先将它除去后再检验.具体步骤如表:
| 实验目的 | 实验步骤 | 实验现象 | 实验结论 |
| 除去干扰物 | ①取广口瓶中溶液少量于试管中,向其中加入过量CaCl2溶液,充分反应后过滤 | 有白色沉淀 产生 | 溶质中还含有NaOH |
| 检验是否 含有NaOH | 在滤液中滴加酚酞试液 | 溶液变红色 |
2.在一定温度下将1mol CO和1mol水蒸气放入一固定容积的密闭容器中,反应CO(g)+H2O(g)?CO2(g)+H2(g)达平衡后,得到0.6mol CO2;再通入0.3mol水蒸气,达到新平衡状态后,CO2的物质的量可能是
( )
( )
| A. | 0.9 mol | B. | 0.8 mol | C. | 0.7 mol | D. | 0.6 mol |
20.Cl2、Br2、I2都具有氧化性,其氧化性Cl2>Br2>I2,Cl2能把溴从溴化物中置换出来,其余依此类推.向NaBr、NaI的混合液中,通入一定量氯气后,将溶液蒸干并充分灼烧,得到固体剩余物质的组成不可能是( )
| A. | NaCl | B. | NaCl NaBr | C. | NaCl NaBr NaI | D. | NaCl NaI |
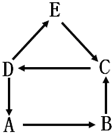 A、B、C、D、E为初中化学常见物质,A是单质,其余为化合物.E可用于检验气体B,它们之间有如图所示的转化关系(“→”表示生成,部分反应物、生成物、反应条件已省略).回答下列问题:
A、B、C、D、E为初中化学常见物质,A是单质,其余为化合物.E可用于检验气体B,它们之间有如图所示的转化关系(“→”表示生成,部分反应物、生成物、反应条件已省略).回答下列问题: