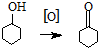题目内容
11.已知下列各反应的焓变①CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H1=-283.0kJ/mol
②H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H2=-285.8kJ/mol
③C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l)△H3=-1370kJ/mol
试求:④2CO(g)+4H2(g)=H2O(l)+C2H5OH(l)△H=-339.2kJ/mol.
分析 根据盖斯定律律①×2-③+②×4构造目标热化学方程式,反应热也乘以相应的系数并进行相应的加减即可,据此进行计算.
解答 解:已知:①CO(g)+1/2O2(g)=CO2(g)△H1=-283.0kJ/mol
②H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H.2=-285.8kJ/mol,
③C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l)△H3=-1370kJ/mol,
根据盖斯定律①×2-③+②×4得:2CO(g)+4H2(g)=H2O(l)+C2H5OH(l)△H.=2△H1-△H3+4△H2;
故△H.4=2△H1-△H3+4△H2=2×(-283.0kJ/mol)-(-1370kJ/mol)+4×(-285.8kJ/mol)=-339.2kJ/mol,
故答案为:-339.2 kJ/mol.
点评 本题考查根据盖斯定律进行的有关反应热的计算,题目难度中等,注意理解盖斯定律,关键是构造目标热化学方程式,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
10.下列属于强电解质的是( )
| A. | NH4Cl | B. | NH3•H2O | C. | Cu | D. | CH3CH2OH |
2.为了提高煤的利用率,人们先把煤转化为CO和H2,再将它们转化为甲醇,某实验人员在一定温度下2L的密闭容器中,充入一定量的H2和CO,发生反应:2H2(g)+CO(g)?CH3OH(g),测定的部分实验数据如下:
(1)在500s内用H2表示的化学反应速率是2.96×10-3mol/(L•s).
(2)在1 000s内用CO表示的化学反应速率是1.26×10-3mol/(L•s),1 000s时CO的转化率是50.4%.
(3)在500s时生成的甲醇的浓度是0.74mol/L.
(4)下列叙述能说明该反应已达到化学平衡状态的是(填标号)ADE;
A.容器内的总压强不随时间而变化
B.反应后混合气体的密度不再发生变化
C.三种气体的浓度相等
D.CH3OH的分解速率与生成速率相等
E.混合气体的平均相对分子质量不再发生变化.
| t/s | 0 | 500 | 1 000 |
| c(H2)/mol•L-1 | 5.00 | 3.52 | 2.48 |
| c(CO)/mol•L-1 | 2.50 |
(2)在1 000s内用CO表示的化学反应速率是1.26×10-3mol/(L•s),1 000s时CO的转化率是50.4%.
(3)在500s时生成的甲醇的浓度是0.74mol/L.
(4)下列叙述能说明该反应已达到化学平衡状态的是(填标号)ADE;
A.容器内的总压强不随时间而变化
B.反应后混合气体的密度不再发生变化
C.三种气体的浓度相等
D.CH3OH的分解速率与生成速率相等
E.混合气体的平均相对分子质量不再发生变化.
6.下列关系不正确的是( )
| A. | 键能:H-F>H-Cl>H-Br>H-I | |
| B. | 还原性:Cl-<Br-<Fe2+<I- | |
| C. | 反应热:C(s)+O2(g)=CO2(g)△H1CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H2△H1>△H2 | |
| D. | 酸性:向次氯酸钠溶液中通入少量的二氧化碳,发生ClO-+CO2+H2O=HCO${\;}_{3}^{-}$+HClO则说明酸性:H2CO3>HClO>HCO${\;}_{3}^{-}$ |
16.下列相关实验中,由“操作和现象”得出的“结论”不正确的是( )
| 操作和现象 | 结论 | |
| A | 取某溶液少许,加入酸化的Ba(NO3)2溶液,产生白色沉淀 | 该溶液一定含SO42- |
| B | NaHCO3溶液与NaAlO2溶液混合产生白色沉淀 | 结合H+的能力:CO32-<AlO2- |
| C | 某溶液加入盐酸产生使石灰水变浑浊的无色无味气体 | 该溶液肯定含HCO3-、CO32-中的一种或二种 |
| D | 测定等浓度的Na2CO3和Na2SO3溶液的pH;前者pH比后者的大; | 非金属性:S>C |
| A. | A | B. | B | C. | C | D. | D |
20.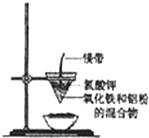 研究性学习小组的同学们用如图所示装置进行铝热反应的实验,请回答:
研究性学习小组的同学们用如图所示装置进行铝热反应的实验,请回答:
(1)氧化铁与铝反应的化学方程式是2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3,
(2)镁带的作用是燃烧时提供热量,引发反应;氯酸钾的作用是受热分解提供氧气,帮助镁条燃烧.
(3)同学们在实验过程中观察到纸漏斗的下部被烧穿,有熔融物落入沙中.他们为探究此熔融物的成分,查阅(化学手册)得知有关物质的熔点、沸点数据如下:
同学们分析数据后推测该熔融物是一种合金,其中的金属是Al、Fe,溶解该合金可选用下列试剂中的BC(填序号).
A.FeSO4溶液 B.稀硫酸 C.稀硝酸 D.NaOH溶液.
 研究性学习小组的同学们用如图所示装置进行铝热反应的实验,请回答:
研究性学习小组的同学们用如图所示装置进行铝热反应的实验,请回答:(1)氧化铁与铝反应的化学方程式是2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3,
(2)镁带的作用是燃烧时提供热量,引发反应;氯酸钾的作用是受热分解提供氧气,帮助镁条燃烧.
(3)同学们在实验过程中观察到纸漏斗的下部被烧穿,有熔融物落入沙中.他们为探究此熔融物的成分,查阅(化学手册)得知有关物质的熔点、沸点数据如下:
| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1462 |
| 沸点/℃ | 2467 | 2980 | 2750 | - |
A.FeSO4溶液 B.稀硫酸 C.稀硝酸 D.NaOH溶液.
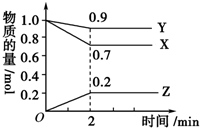 某温度时,在2L容器中,X、Y、Z三种物质的物质的量随时间变化曲线如图所示.由图中数据分析,该反应的化学方程式为Y+3X?2Z,反应开始至2min,X的转化率为30%.
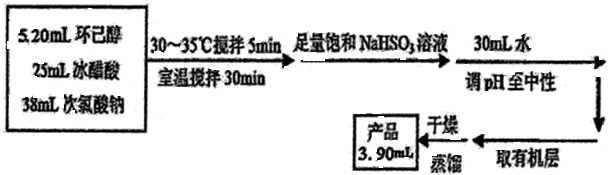
某温度时,在2L容器中,X、Y、Z三种物质的物质的量随时间变化曲线如图所示.由图中数据分析,该反应的化学方程式为Y+3X?2Z,反应开始至2min,X的转化率为30%.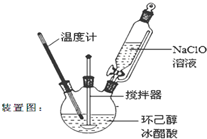 环己酮是重要化工原料,是制造尼龙、己内酰胺和己二酸的主要中间体.某化学兴趣小组尝试用次氯酸钠制备环己酮.方程式为:
环己酮是重要化工原料,是制造尼龙、己内酰胺和己二酸的主要中间体.某化学兴趣小组尝试用次氯酸钠制备环己酮.方程式为: