题目内容
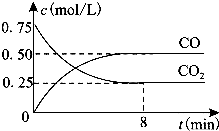 一定条件下铁可以和CO2发生反应:Fe(s)+CO2(g)=FeO(s)+CO(g)△H>0,1100℃时,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和CO气体的浓度与时间的关系如图所示.
一定条件下铁可以和CO2发生反应:Fe(s)+CO2(g)=FeO(s)+CO(g)△H>0,1100℃时,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和CO气体的浓度与时间的关系如图所示.(1)下列措施中能使平衡时K增大的是
A.升高温度 B.增大压强 C.充入一定量CO D.降低温度
(2)8分钟内,CO的平均反应速率v(CO)=
(3)1100℃时,2L的密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如表
| 容器 | 甲 | 乙 |
| 反应物投入量 | 3mol Fe、2mo lCO2 | 4mol FeO、3mol CO |
| CO的浓度(mol?L-1) | c1 | c2 |
| CO2的体积分数 | φ1 | φ2 |
| 体系压强(Pa) | P1 | P2 |
| 气态反应物的转化率 | a1 | a2 |
A.2c1=3c2 B.φ1=φ2 C.P1<P2 D.a1=a2
②求c1=
考点:物质的量或浓度随时间的变化曲线,等效平衡
专题:化学平衡专题
分析:(1)平衡常数随温度变化,结合平衡移动原理分析判断;
(2)8分钟内,一氧化碳难度变化0.5mol/L,依据V=
计算CO的平均反应速率;
(3)Fe(s)+CO2(g)?FeO(s)+CO(g),反应是气体体积不变的吸热反应,
①依据图表数据分析,反应前后气体体积不变,加入2molCO2,加入3mol CO,相当于加入3molCO2,的平衡状态,气体物质条件分数相同,物质的量不同,压强不同,气体物质的量大的容器中压强大,起始量不同,平衡浓度、转化率不同;
②依据题干计算平衡常数,结合化学平衡三段式列式计算.
(2)8分钟内,一氧化碳难度变化0.5mol/L,依据V=
| △c |
| △t |
(3)Fe(s)+CO2(g)?FeO(s)+CO(g),反应是气体体积不变的吸热反应,
①依据图表数据分析,反应前后气体体积不变,加入2molCO2,加入3mol CO,相当于加入3molCO2,的平衡状态,气体物质条件分数相同,物质的量不同,压强不同,气体物质的量大的容器中压强大,起始量不同,平衡浓度、转化率不同;
②依据题干计算平衡常数,结合化学平衡三段式列式计算.
解答:
解:(1)平衡常数随温度变化,不随浓度压强等因素变化,反应是吸热反应,升温平衡时K增大;
A.升高温度,平衡正向进行,平衡常数增大,故A正确;
B.增大压强,平衡不动,平衡常数不变,故B错误;
C.充入一定量CO,平衡逆向进行,但平衡常数不变,故C错误;
D.降低温度,平衡逆向进行,平衡常数减小,故D错误;
故答案为:A;
(2)依据图象分析,8分钟内,一氧化碳浓度变化0.5mol/L,CO的平均反应速率v(CO)=
=0.0625mol/L?min;
故答案为:0.0625;
(3)①依据图表数据分析,反应前后气体体积不变,加入2molCO2,加入3mol CO,相当于加入3molCO2,平衡时气体体积分数相同,物质的量不同,压强不同,气体物质的量大的容器中压强大,起始量不同,平衡浓度、转化率不同;
A.达到平衡状态,一氧化碳的浓度关系为:3c1=2c2,故A错误;
B.反应物和生成物都是一种,平衡常数相同,所以达到平衡状态二氧化碳的体积分数相同,φ1=φ2,故B正确;
C.乙容器中气体物质的量大于甲容器,所以达到平衡状态p1<p2,故C正确;
D.起始量不同,甲容器正向进行,乙容器逆向进行,气态反应物的转化率不同,故D错误;
故答案为:BC;
②图象分析反应在1100°C反应的平衡常数K=
=2
甲容器中设反应的二氧化碳浓度为x,
Fe(s)+CO2(g)?FeO(s)+CO(g),
起始量(mol/L) 1 0
变化量(mol/L) x x
平衡量(mol/L) 1-x x
K=
=2
x=
mol/L
平衡状态CO的浓度=
(mol/L)=0.67mol/L,
CO2的体积分数φ1=
×100%=
×100%=33.3%;
乙容器中温度和甲容器相同,平衡常数相同,所以二氧化碳的体积分数φ2=φ1 =33.3%;
故答案为:0.67mol/L;33.3% 33.3%.
A.升高温度,平衡正向进行,平衡常数增大,故A正确;
B.增大压强,平衡不动,平衡常数不变,故B错误;
C.充入一定量CO,平衡逆向进行,但平衡常数不变,故C错误;
D.降低温度,平衡逆向进行,平衡常数减小,故D错误;
故答案为:A;
(2)依据图象分析,8分钟内,一氧化碳浓度变化0.5mol/L,CO的平均反应速率v(CO)=
| 0.5mol/L |
| 8min |
故答案为:0.0625;
(3)①依据图表数据分析,反应前后气体体积不变,加入2molCO2,加入3mol CO,相当于加入3molCO2,平衡时气体体积分数相同,物质的量不同,压强不同,气体物质的量大的容器中压强大,起始量不同,平衡浓度、转化率不同;
A.达到平衡状态,一氧化碳的浓度关系为:3c1=2c2,故A错误;
B.反应物和生成物都是一种,平衡常数相同,所以达到平衡状态二氧化碳的体积分数相同,φ1=φ2,故B正确;
C.乙容器中气体物质的量大于甲容器,所以达到平衡状态p1<p2,故C正确;
D.起始量不同,甲容器正向进行,乙容器逆向进行,气态反应物的转化率不同,故D错误;
故答案为:BC;
②图象分析反应在1100°C反应的平衡常数K=
| 0.50 |
| 0.25 |
甲容器中设反应的二氧化碳浓度为x,
Fe(s)+CO2(g)?FeO(s)+CO(g),
起始量(mol/L) 1 0
变化量(mol/L) x x
平衡量(mol/L) 1-x x
K=
| x |
| 1-x |
x=
| 2 |
| 3 |
平衡状态CO的浓度=
| 2 |
| 3 |
CO2的体积分数φ1=
| 1-x |
| x |
| 1 |
| 3 |
乙容器中温度和甲容器相同,平衡常数相同,所以二氧化碳的体积分数φ2=φ1 =33.3%;
故答案为:0.67mol/L;33.3% 33.3%.
点评:本题考查化学平衡影响因素、等效平衡、化学平衡的计算,题目计算量较大,难度较大,关键是构建平衡建立的等效途径.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列反应中,反应物和产物的空间构型不会发生本质变化的是( )
A、CH4
| |||
B、CH2═CH2
| |||
C、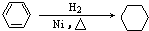 | |||
D、CH4
|

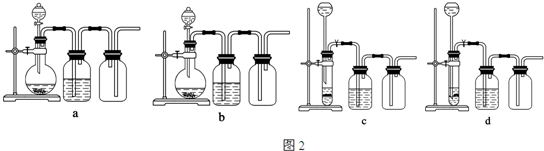
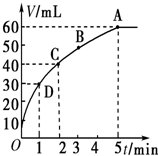 把0.01mol MnO2粉末加入50mL过氧化氢的溶液里,在标准状况下,放出气体的体积V和时间t的关系曲线如图所示.
把0.01mol MnO2粉末加入50mL过氧化氢的溶液里,在标准状况下,放出气体的体积V和时间t的关系曲线如图所示.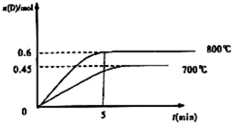 在容积为1L的密闭容器中,进行反应:A(g)+2B(g)?C(g)+D(g),在不同温度下,D的物质的量n(D)和时间t的关系如图.试回答下列问题:
在容积为1L的密闭容器中,进行反应:A(g)+2B(g)?C(g)+D(g),在不同温度下,D的物质的量n(D)和时间t的关系如图.试回答下列问题: