题目内容
下列说法正确的是( )
| A、1 L水中溶解了58.5 g NaCl,该溶液的物质的量浓度为1 mol/L |
| B、从1 L 2 mol/L的H2SO4溶液中取出0.5 L,该溶液的浓度为1 mol/L |
| C、配制500 mL 0.5 mol/L的CuSO4溶液,需62.5 g胆矾 |
| D、中和100 mL 1 mol/L的H2SO4溶液,需NaOH为4 g |
考点:物质的量浓度的相关计算
专题:计算题
分析:A.58.5 g NaCl的物质的量为1mol,溶于水配成1L溶液,所得溶液浓度为1 mol/L;
B.溶液是均匀的,取出的0.5L硫酸溶液的浓度与原溶液浓度相等;
C.根据n=cV计算硫酸铜的物质的量,硫酸铜与胆矾物质的量相等,再根据m=nM计算胆矾的质量;
D.根据n=cV计算硫酸的物质的量,根据方程式计算NaOH的物质的量,再根据m=nM计算氢氧化钠的质量.
B.溶液是均匀的,取出的0.5L硫酸溶液的浓度与原溶液浓度相等;
C.根据n=cV计算硫酸铜的物质的量,硫酸铜与胆矾物质的量相等,再根据m=nM计算胆矾的质量;
D.根据n=cV计算硫酸的物质的量,根据方程式计算NaOH的物质的量,再根据m=nM计算氢氧化钠的质量.
解答:
解:A.58.5 g NaCl的物质的量为1mol,溶于水配成1L溶液,所得溶液浓度为1 mol/L,体积1L是指溶液的体积,不是溶剂水的体积,故A错误;
B.溶液是均匀的,取出的0.5L硫酸溶液的浓度与原溶液浓度相等为1mol/L,故B错误;
C.硫酸铜的物质的量=0.5L×0.5mol/L=0.25mol,硫酸铜与胆矾物质的量相等,故需要胆矾的质量=0.25mol×250g/mol=62.5g,故C正确;
D.硫酸的物质的量=0.1L×1mol/L=0.1mol,根据方程式H2SO4+2NaOH=Na2SO4+2H2O,可知需NaOH的物质的量为0.1mol×2=0.2mol,故需要NaOH的质量=0.2mol×40g/mol=8g,故D错误,
故选C.
B.溶液是均匀的,取出的0.5L硫酸溶液的浓度与原溶液浓度相等为1mol/L,故B错误;
C.硫酸铜的物质的量=0.5L×0.5mol/L=0.25mol,硫酸铜与胆矾物质的量相等,故需要胆矾的质量=0.25mol×250g/mol=62.5g,故C正确;
D.硫酸的物质的量=0.1L×1mol/L=0.1mol,根据方程式H2SO4+2NaOH=Na2SO4+2H2O,可知需NaOH的物质的量为0.1mol×2=0.2mol,故需要NaOH的质量=0.2mol×40g/mol=8g,故D错误,
故选C.
点评:本题考查对物质的量浓度理解及有关计算,比较基础,侧重对基础知识的巩固.

练习册系列答案
相关题目
有关合金的描述正确的是( )
①合金的硬度一般比它的各成分金属的大;
②合金的熔点一般比它的各成分金属的更低;
③改变原料的配比、改变生成合金的条件,得到有不同性能的合金;
④合金中至少含两种金属;⑤合金中一定含有金属.
①合金的硬度一般比它的各成分金属的大;
②合金的熔点一般比它的各成分金属的更低;
③改变原料的配比、改变生成合金的条件,得到有不同性能的合金;
④合金中至少含两种金属;⑤合金中一定含有金属.
| A、①②③⑤ | B、②③④ |
| C、①②④ | D、①②④⑤ |
下列各项表达中正确的是( )
A、Na2O2的电子式为 |
| B、二氧化硅的分子式为SiO2 |
C、氦原子的电子排布图为  |
D、Cl-的结构示意图为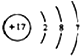 |
设NA表示阿伏加德罗常数,下列物质中物质的量为1摩尔的是( )
| A、通常状况下22.4 L氯气 |
| B、4℃时18毫升水 |
| C、含2NA 个氦原子的氦气 |
| D、标准状况下22.4 L H2O |
容量瓶上未必有固定的( )
| A、溶液浓度 | B、容量 |
| C、定容刻度 | D、配制温度 |
四氟乙烯(CF2=CF2)可以看作是乙烯分子中的所有氢原子被氟原子取代,它和乙烯性质相似.聚四氟乙烯可做家用不粘锅的内衬.下列说法正确的是( )
| A、四氟乙烯不能使溴水褪色 |
| B、四氟乙烯分子中所有原子在同一平面 |
| C、聚四氟乙烯的性质活泼,易燃易爆 |
| D、聚四氟乙烯可由乙烯和氟气(F2)加成制得 |
NA代表阿伏加德罗常数,下列说法正确的是( )
| A、0.5 mol Al与足量盐酸反应转移电子数为1.5NA |
| B、标准状况下,11.2 L SO3所含的分子数为0.5NA |
| C、0.5 mol CH4所含的电子数为2.5NA |
| D、46 g NO2和N2O4的混合物含有的分子数为1NA |