题目内容
15.稀硫酸酸化后的软锰矿(主要成分为MnO2 )悬浊液可用于吸收燃煤尾气中的SO2,得到MnSO4;MnSO4可与KMnO4反应制备电池材料MnO2,同时生成H2SO4.下列用来解释事实的方程式不正确的是( )| A. | MnO2吸收SO2的反应:MnO2+SO2═MnSO4 | |
| B. | MnO2作为碱性电池正极材料时的放电反应:MnO2+e-+H+═MnOOH | |
| C. | MnSO4与KMnO4反应制备MnO2:2MnO4-+3Mn2++2H2O═5MnO2+4H+ | |
| D. | 尾气中的SO2 还可用足量的氨水吸收:SO2+2NH3•H2O═2NH4++SO32-+H2O |
分析 A.S元素被二氧化锰氧化为硫酸根离子;
B.碱性条件下,电极方程式中不能有氢离子参加;
C.MnSO4与KMnO4反应生成MnO2;
D.SO2是酸性气体,与氨水反应生成盐溶液.
解答 解:A.S元素被二氧化锰氧化为硫酸根离子,则MnO2吸收SO2的反应:MnO2+SO2═MnSO4,故A正确;
B.碱性条件下,电极方程式中不能有氢离子参加,所以MnO2作为碱性电池正极材料时的放电反应:MnO2+e-+H2O═MnOOH+OH-,故B错误;
C.MnSO4被KMnO4氧化生成MnO2,则MnSO4与KMnO4反应制备MnO2:2MnO4-+3Mn2++2H2O═5MnO2+4H+,故C正确;
D.SO2是酸性气体,与氨水反应生成盐溶液,所以尾气中的SO2 还可用足量的氨水吸收:SO2+2NH3•H2O═2NH4++SO32-+H2O,故D正确.
故选B.
点评 本题考查了元素化合物的性质、氧化还原反应、离子方程式的书写,题目难度中等,侧重于基础知识的综合应用的考查,注意溶液的酸碱性对电极方程式的影响.

练习册系列答案
相关题目
5.下列方法正确的是( )
①用过滤的方法除去食盐水中的泥沙
②用蒸馏的方法将自来水制成蒸馏水
③用酒精萃取碘水中的碘
④用淘洗的方法从沙里淘金.
①用过滤的方法除去食盐水中的泥沙
②用蒸馏的方法将自来水制成蒸馏水
③用酒精萃取碘水中的碘
④用淘洗的方法从沙里淘金.
| A. | ②③④ | B. | ①②④ | C. | ①③④ | D. | ①②③ |
3.比较下面各组热化学方程式,△H1<△H2的是( )
| A. | 2H2(g)+O2(g)=2H2O(g )△H1 2H2(g)+O2(g)=2H2O(1)△H2 | |
| B. | S(g)+O2(g)=SO2(g )△H1 S(s)+O2(g)=SO2(g )△H2 | |
| C. | C(s)+$\frac{1}{2}$O2(g)=CO (g )△H1 C(s)+O2(g)=CO2 (g )△H2 | |
| D. | H2(g)+Cl2(g)=2HCl(g )△H1 $\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)=HCl(g )△H2 |
10.1898年,居里夫人经过一段漫长、枯燥而又艰苦的工作,终于从数吨沥青铀矿中提炼出一小撮放射性粉末,并分离出了两种放射性元素钋和镭,其中镭是元素周期表中第7周期ⅡA族的元素.下列关于镭的性质描述中不正确的是( )
| A. | 在化合物中呈现+2价 | B. | 氢氧化物呈强碱性 | ||
| C. | 单质与冷水不反应 | D. | 碳酸盐难溶于水 |
20.如图,有关零排放车载燃料电池叙述正确的是( )


| A. | 正极通入H2,发生还原反应 | |
| B. | 负极通入H2,发生还原反应 | |
| C. | 总反应式为2H2+O2=2H2O | |
| D. | 导电离子为质子,且在电池内部由正极定向移向负极 |
7.部分难溶物的颜色和常温下的Ksp如下表所示:
某研究性学习小组对电解食盐水进行了如下探究: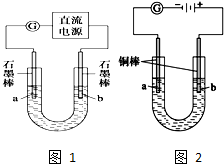
实验Ⅰ:装置如图所示,接通电源后,发现a、b电极上均有气泡产生.
(1)电解过程中的总离子反应方程式为2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑.
(2)为了确定电源的正、负极,下列操作一定行之有效的是BD.
A.观察两极产生气体的颜色
B.往U形管两端分别滴入数滴酚酞试液
C.用燃着的木条靠近U形管口
D.在U形管口置一张湿润的淀粉KI试纸
实验Ⅱ:把上述电解装置的石墨棒换成铜棒,用直流电源进行电解,装置如图所示.
观察到的现象如下所示:
①开始无明显现象,随后液面以下的铜棒表面逐渐变暗;
②5min后,b极附近开始出现白色沉淀,并逐渐增多,且向a极扩散;
③10min后,最靠近a极的白色沉淀开始变成红色;
④12min后,b极附近的白色沉淀开始变成黄色,然后逐渐变成橙黄色;
⑤a极一直有大量气泡产生;
⑥停止电解,将U形管中悬浊液静置一段时间后,上层溶液呈无色,没有出现蓝色,下层沉淀全部显砖红色.
(3)a极发生的电极反应方程式为:2H++2e-=H2↑(或2H2O+2e-═2OH-+H2↑).
(4)电解5min后,b极发生的电极反应方程式为:Cu+Cl--e-═CuCl↓.
(5)12min后,b极附近出现的橙黄色沉淀的成分是CuOH和Cu2O,原因是Ksp(CuOH)<Ksp(CuCl),CuCl转化为黄色的CuOH沉淀,CuOH不稳定分解生成Cu2O,所以橙黄色沉淀的成分为CuOH和Cu2O的混合物.
| Cu(OH)2 | CuOH | CuCl | Cu2O | |
| 颜色 | 蓝色 | 黄色 | 白色 | 砖红色 |
| Ksp(25℃) | 1.6×10-19 | 1.0×10-14 | 1.2×10-6 | - |

实验Ⅰ:装置如图所示,接通电源后,发现a、b电极上均有气泡产生.
(1)电解过程中的总离子反应方程式为2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑.
(2)为了确定电源的正、负极,下列操作一定行之有效的是BD.
A.观察两极产生气体的颜色
B.往U形管两端分别滴入数滴酚酞试液
C.用燃着的木条靠近U形管口
D.在U形管口置一张湿润的淀粉KI试纸
实验Ⅱ:把上述电解装置的石墨棒换成铜棒,用直流电源进行电解,装置如图所示.
观察到的现象如下所示:
①开始无明显现象,随后液面以下的铜棒表面逐渐变暗;
②5min后,b极附近开始出现白色沉淀,并逐渐增多,且向a极扩散;
③10min后,最靠近a极的白色沉淀开始变成红色;
④12min后,b极附近的白色沉淀开始变成黄色,然后逐渐变成橙黄色;
⑤a极一直有大量气泡产生;
⑥停止电解,将U形管中悬浊液静置一段时间后,上层溶液呈无色,没有出现蓝色,下层沉淀全部显砖红色.
(3)a极发生的电极反应方程式为:2H++2e-=H2↑(或2H2O+2e-═2OH-+H2↑).
(4)电解5min后,b极发生的电极反应方程式为:Cu+Cl--e-═CuCl↓.
(5)12min后,b极附近出现的橙黄色沉淀的成分是CuOH和Cu2O,原因是Ksp(CuOH)<Ksp(CuCl),CuCl转化为黄色的CuOH沉淀,CuOH不稳定分解生成Cu2O,所以橙黄色沉淀的成分为CuOH和Cu2O的混合物.
4.将两个铂电极插入KOH溶液中,向两极分别通入CH4和O2即可构成甲烷燃料电池.已知电池的总反应为CH4+2O2+2OH-=CO32-+3H2O,下列叙述正确的是( )
| A. | 通入甲烷的一极为正极,该极c(OH-)减小 | |
| B. | 通入甲烷的一极的电极反应为CH4-8e-+3H2O=CO32-+10H+ | |
| C. | 通入氧气一极发生还原反应,电极反应为O2+2H2O+4e-=4OH- | |
| D. | 该电池工作时,溶液中的阴离子向正极移动 |
6.下列物质肯定是纯净物的是( )
| A. | 汽油 | B. | 化学式为C2H6O的物质 | ||
| C. | 聚乙烯 | D. | 化学式为CH2Cl2的物质 |
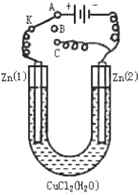 在一个U形管里盛有氯化铜溶液,并插入两块锌片作电极,按如图连接:
在一个U形管里盛有氯化铜溶液,并插入两块锌片作电极,按如图连接: