题目内容
20.如图,有关零排放车载燃料电池叙述正确的是( )
| A. | 正极通入H2,发生还原反应 | |
| B. | 负极通入H2,发生还原反应 | |
| C. | 总反应式为2H2+O2=2H2O | |
| D. | 导电离子为质子,且在电池内部由正极定向移向负极 |
分析 氢氧燃料电池中,通入燃料氢气的电极是负极,发生氧化反应、通入氧化剂氧气的电极是正极发生还原反应,阳离子移向正极,阴离子移向负极,总反应即燃料燃烧反应,据此分析解答.
解答 解:A.燃料电池中,负极上通入燃料、正极上通入氧化剂,所以正极通入氧气,发生还原反应,故A错误;
B.燃料电池中,负极上通入燃料,所以负极通入H2,发生氧化反应,故B错误;
C.总反应即燃料燃烧反应即2H2+O2=2H2O,故C正确;
D.导电离子为质子,质子带正电荷,应由负极移向正极,故D错误;
故选C.
点评 本题考查化学电源新型电池,题目难度不大,明确原电池原理是解本题关键,所有燃料电池中都是负极上通入燃料、正极上通入氧化剂,会根据溶液酸碱性书写电极反应式.

练习册系列答案
相关题目
10.把少量的氯水滴加到过量的KI溶液中,再加入四氯化碳,振荡后静置,下列现象中正确的是( )
| A. | 得到均匀的紫色溶液 | B. | 无色水层下有橙红色液体 | ||
| C. | 无色水层下有紫色油状液体 | D. | 无色水层上有紫色油状液体 |
11.X、Y、Z、W是元素周期表前四周期中常见的元素,其相关信息如下表:
(1)W位于元素周期表第四周期第Ⅷ族.
(2)X的电负性比Y的小(填“大”或“小”);
(3)X 和Y的气态氢化物中,熔沸点较高的是H2O(写化学式).原因:H2O分子间形成氢键
(4)写出Z2Y2与XY2反应的化学方程式,并标出电子转移的方向和数目: .
.
| 元素 | 相关信息 |
| X | X的基态原子L层电子数是K层电子数的2倍 |
| Y | Y的基态原子最外层电子排布式为:nsnnpn+2 |
| Z | Z存在质量数为23,中子数为12的核素 |
| W | W有多种化合价,其白色氢氧化合物在空气中会迅速变成灰绿色,最后变成红褐色 |
(2)X的电负性比Y的小(填“大”或“小”);
(3)X 和Y的气态氢化物中,熔沸点较高的是H2O(写化学式).原因:H2O分子间形成氢键
(4)写出Z2Y2与XY2反应的化学方程式,并标出电子转移的方向和数目:
 .
.
8.下列分子种的碳原子不可能同在一个平面的是( )
| A. | 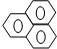 | B. | 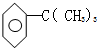 | C. | 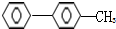 | D. | 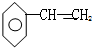 |
15.稀硫酸酸化后的软锰矿(主要成分为MnO2 )悬浊液可用于吸收燃煤尾气中的SO2,得到MnSO4;MnSO4可与KMnO4反应制备电池材料MnO2,同时生成H2SO4.下列用来解释事实的方程式不正确的是( )
| A. | MnO2吸收SO2的反应:MnO2+SO2═MnSO4 | |
| B. | MnO2作为碱性电池正极材料时的放电反应:MnO2+e-+H+═MnOOH | |
| C. | MnSO4与KMnO4反应制备MnO2:2MnO4-+3Mn2++2H2O═5MnO2+4H+ | |
| D. | 尾气中的SO2 还可用足量的氨水吸收:SO2+2NH3•H2O═2NH4++SO32-+H2O |