题目内容
6.在相同温度时,100mL0.01mol•L-1的氨水溶液与10mL 0.1mol•L-1的氨水溶液相比较,下列数值中,前者大于后者的是( )| A. | 中和时所需HCl的量 | B. | NH3•H2O的电离常数 | ||
| C. | OH-的物质的量 | D. | OH-的浓度 |
分析 根据氨水的浓度越小,其电离程度越大,但溶液的浓度小,电离产生的离子的浓度小,据此分析.
解答 解:A.由n=cV可知,100mL 0.01mol/L的NH3•H2O与10mL0.1mol/L的NH3•H2O中溶质的物质的量都是0.001mol,则中和时所需HCl的量相等,故A错误;
B.电离常数只与温度有关,温度相同,电离常数相同,故B错误;
C.溶液越稀,电解质的电离程度越大,所以OH-的物质的量前者大于后者,故C正确;
D.相同温度下,0.01mol/L的NH3•H2O小于0.1mol/L的NH3•H2O的浓度,则前者电离产生的氢氧根离子浓度小于后者,故D错误.
故选C.
点评 本题考查弱电解质的电离,题目难度不大,本题注意一水合氨为弱电解质,浓度不同,电离程度不同,浓度越大,电离程度越小的特征.

练习册系列答案
 步步高达标卷系列答案
步步高达标卷系列答案
相关题目
7.下列说法正确的是( )
| A. | ${\;}_{8}^{16}$O、${\;}_{8}^{17}$O、${\;}_{8}^{18}$O互为同素异形体 | |
| B. | O2与O3互为同位素 | |
| C. | CH3-CH2-OH与CH3-O-CH3互为分异构体 | |
| D. | H2O与D2O互为同分异构体 |
17.下列说法正确的是( )
| A. | 常温下,将pH=3的醋酸溶液稀释到原体积的10倍后,溶液的pH=4 | |
| B. | 为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH.若pH>7,则H2A是弱酸;若pH<7,则H2A是强酸 | |
| C. | 用0.2000 mol•L-1 NaOH标准溶液滴定HCl与CH3COOH的混合液(混合液中两种酸的浓度均约为0.1 mol•L-1),当pH=7时,溶液中的酸恰好完全中和 | |
| D. | 相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水、②0.1 mol•L-1盐酸、③0.1 mol•L-1氯化镁溶液、④0.1 mol•L-1硝酸银溶液中,Ag+浓度:④>①>②>③ |
14.对于常温下pH=12的氨水,下列说法正确的是( )
| A. | 由水电离产生的c(OH-)=10-12mol•L-1 | |
| B. | 向溶液中加入等体积的pH=2盐酸后溶液呈酸性 | |
| C. | 向溶液中加入稀盐酸可以促进氨水的电离,溶液的碱性增强 | |
| D. | 向溶液中加入适量盐酸使混合液的pH=7,混合液中c(NH4+)>c(Cl-) |
1. 25℃,电离平衡常数:
25℃,电离平衡常数:
回答下列问题:
(1)物质的量浓度为0.1mol/L的下列四种物质:a.Na2CO3,b.NaClO,c.CH3COONa,d.NaHCO3;pH由大到小的顺序是abdc(填编号)
(2)在Na2CO3溶液中通入少量的SO2气体,写出离子方程式2CO32-+SO2+H2O═2HCO3-+SO32-
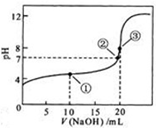
(3)用0.1000mol/L NaOH溶液滴定0.1000mol/L 20mL CH3COOH溶液,得到如图曲线在②时,溶液中离子浓度大小顺序为c(Na+)=c(CH3COO-)>c(H+)=c(OH-)
在①时,测得pH约为5,c(CH3COO-)-c(Na+)=10-5-10-9mol/L(填精确数值)
(4)常温下,CH3COOH与NH3.H2O的电离平衡常数均为1.8×10-5,则NH4HCO3溶液呈碱性.
溴水.
 25℃,电离平衡常数:
25℃,电离平衡常数:| 化学式 | CH3COOH | H2CO3 | HClO | H2SO3 |
| 电离平衡常数 | 1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 | K1=1.5×10-2 K2=1.0×10-7 |
(1)物质的量浓度为0.1mol/L的下列四种物质:a.Na2CO3,b.NaClO,c.CH3COONa,d.NaHCO3;pH由大到小的顺序是abdc(填编号)
(2)在Na2CO3溶液中通入少量的SO2气体,写出离子方程式2CO32-+SO2+H2O═2HCO3-+SO32-
(3)用0.1000mol/L NaOH溶液滴定0.1000mol/L 20mL CH3COOH溶液,得到如图曲线在②时,溶液中离子浓度大小顺序为c(Na+)=c(CH3COO-)>c(H+)=c(OH-)
在①时,测得pH约为5,c(CH3COO-)-c(Na+)=10-5-10-9mol/L(填精确数值)
(4)常温下,CH3COOH与NH3.H2O的电离平衡常数均为1.8×10-5,则NH4HCO3溶液呈碱性.
溴水.
18.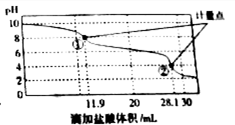 称取Na2CO3和NaHCO3混合物样品1.6226g,溶于水配成250.00ml溶液,取出该溶液25.00ml用 0.1mol•L-1 盐酸滴定,得到如图曲线.以下说法错误的是( )
称取Na2CO3和NaHCO3混合物样品1.6226g,溶于水配成250.00ml溶液,取出该溶液25.00ml用 0.1mol•L-1 盐酸滴定,得到如图曲线.以下说法错误的是( )
 称取Na2CO3和NaHCO3混合物样品1.6226g,溶于水配成250.00ml溶液,取出该溶液25.00ml用 0.1mol•L-1 盐酸滴定,得到如图曲线.以下说法错误的是( )
称取Na2CO3和NaHCO3混合物样品1.6226g,溶于水配成250.00ml溶液,取出该溶液25.00ml用 0.1mol•L-1 盐酸滴定,得到如图曲线.以下说法错误的是( )| A. | 样品中Na2CO3含量越高,起始pH也越大 | |
| B. | 计量点①中有关离子浓度关系为:c(HCO3-)>C(Cl-)>c(CO32-) | |
| C. | 计量点②溶液中有关离子浓度关系为:2(CO32-)+c(HCO3-)=C(H+)-c(OH-) | |
| D. | 此样品n(NaHCO3)=(28.1-11.9)×10-3mol |
15.目前污水处理厂用新型高效絮凝剂碱式硫酸铁[Fe(OH)SO4]来处理水中的悬浮颗粒物,采用微生物燃料电池使水中的有机物变成二氧化碳,从而使污水得到净化.
I.工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的工艺流程如图1:
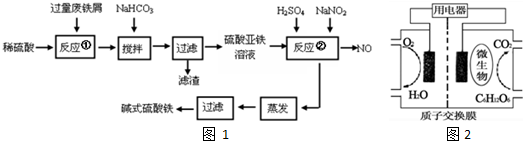
已知:25℃时部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
回答下列问题:
(1)加入少量NaHCO3的目的是调节pH在4.4-7.5范围内,使溶液中Al 3+沉淀.
(2)若沉淀完全时溶液中金属离子浓度为1.0×10-5mol/L,则Ksp[Fe(OH)2]=1.0×10-15.
(3)在实际生产中,反应②常同时通入O2以减少NaNO2的用量,若标况下有33.6L O2参与反应,则相当于节约NaNO2的物质的量为6mol.
(4)该生产碱式硫酸铁的工艺过程中存在的明显缺点是会产生一氧化氮,会造成大气污染.
II.微生物燃料电池是以微生物作催化剂,以有机污水为燃料,将有机污水中的化学能直接转化为电能的一种装置.
(5)重庆大学研究出一种微生物燃料电池,可以将污水中的CH3COO-处理掉,
其总反应为:2CH3COOK+4H2O+8K2S2O8═4CO2↑+7H2SO4+9K2SO4,写出该微生物
燃料电池负极的电极反应式CH3COO-+2H2O-8e-=2CO2↑+7H+.
(6)以葡萄糖为燃料的微生物燃料电池结构示意图如图2:
①关于该电池的叙述,正确的有BD
A.电池的正极反应为:O2+2H2O+4e-═4OH-
B.在电池反应中,每消耗90克葡萄糖,经外电路通过的电子数为12NA
C.该电池能够在高温下工作
D.放电过程中,H+从负极区向正极区迁移
②化学需氧量(COD)是重要的水质指标,其数值表示将1L水中的有机物氧化为CO2、H2O所需消耗的氧气的质量.利用微生物燃料电池来处理某些污水并进行发电,如果1L废水中有机物(折算成葡萄糖)氧化所提供的化学能低于5.6kJ,就没有
发电的价值.则适合用微生物燃料电池发电的污水,其COD最低为384mg/L.
(已知葡萄糖的燃烧热为2800kJ/mol)
I.工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的工艺流程如图1:

已知:25℃时部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.0 | 4.4 |
(1)加入少量NaHCO3的目的是调节pH在4.4-7.5范围内,使溶液中Al 3+沉淀.
(2)若沉淀完全时溶液中金属离子浓度为1.0×10-5mol/L,则Ksp[Fe(OH)2]=1.0×10-15.
(3)在实际生产中,反应②常同时通入O2以减少NaNO2的用量,若标况下有33.6L O2参与反应,则相当于节约NaNO2的物质的量为6mol.
(4)该生产碱式硫酸铁的工艺过程中存在的明显缺点是会产生一氧化氮,会造成大气污染.
II.微生物燃料电池是以微生物作催化剂,以有机污水为燃料,将有机污水中的化学能直接转化为电能的一种装置.
(5)重庆大学研究出一种微生物燃料电池,可以将污水中的CH3COO-处理掉,
其总反应为:2CH3COOK+4H2O+8K2S2O8═4CO2↑+7H2SO4+9K2SO4,写出该微生物
燃料电池负极的电极反应式CH3COO-+2H2O-8e-=2CO2↑+7H+.
(6)以葡萄糖为燃料的微生物燃料电池结构示意图如图2:
①关于该电池的叙述,正确的有BD
A.电池的正极反应为:O2+2H2O+4e-═4OH-
B.在电池反应中,每消耗90克葡萄糖,经外电路通过的电子数为12NA
C.该电池能够在高温下工作
D.放电过程中,H+从负极区向正极区迁移
②化学需氧量(COD)是重要的水质指标,其数值表示将1L水中的有机物氧化为CO2、H2O所需消耗的氧气的质量.利用微生物燃料电池来处理某些污水并进行发电,如果1L废水中有机物(折算成葡萄糖)氧化所提供的化学能低于5.6kJ,就没有
发电的价值.则适合用微生物燃料电池发电的污水,其COD最低为384mg/L.
(已知葡萄糖的燃烧热为2800kJ/mol)
16.化学与环境保护密切相关,下列说法不正确的是( )
| A. | PM2.5是指大气中直径≤2,5微米的颗粒物也称为可入肺颗粒物,对人体危害最大是因为它可以直接进入肺泡 | |
| B. | 雾霾是因为汽车排放尾气,工厂排放废气,燃烧烟花爆竹、烹饪等原因所造成的 | |
| C. | 化石能源不仅不可再生,而且在燃烧过程中会产生染污性物质,因此应不再使用化石能源,这符合绿色化学的核心 | |
| D. | 对煤进行气化、液化、脱硫等处理,不仅可以提高其利用率,而且可以降低对环境的污染 |