题目内容
8.化学在环境保护中起着十分重要的作用,电化学降解MO3-的原理如图所示:则下列判断正确的是
| A. | 电源正极为B | |
| B. | 若电解过程中转移了1mol电子,则膜两侧电解液的质量变化差(|△m左|-|△m右|)为7.2克 | |
| C. | Pt电极上产物为H2 | |
| D. | Ag-Pt电极上发生氧化反应 |
分析 由图示知在Ag-Pt电极上NO3-发生还原反应,因此Ag-Pt电极为阴极,则B为负极,A为电源正极;阴极反应是NO3-得电子发生还原反应生成N2,转移1mol电子时,阳极(阳极反应为H2O失电子氧化为O2和H+)消耗0.5mol水,产生1molH+进入阴极室,阳极室质量减少9g;阴极室中放出0.1molN2(2.8g),同时有1molH+(1g)进入阴极室,以此解答该题.
解答 解:A.该装置中,硝酸根离子得电子发生还原反应,则Ag-Pt电极为阴极、Pt电极为阳极,连接阴极的B电极为负极,A为正极,故A错误;
B.转移1mol电子时,阳极(阳极反应为H2O失电子氧化为O2和H+)消耗0.5mol水,产生1molH+进入阴极室,阳极室质量减少9g;阴极室中放出0.1molN2(2.8g),同时有1molH+(1g)进入阴极室,因此阴极室质量减少1.8g,故膜两侧电解液的质量变化差(△m左-△m右)=9g-1.8g=7.2g,故B正确;
C.Pt电极为阳极,发生氧化反应,氢氧根离子放电,产生氧气,故C错误;
D.由图示知在Ag-Pt电极上NO3-发生还原反应,因此Ag-Pt电极为阴极,阴极上硝酸根离子得电子发生还原反应,故D错误.
故选B.
点评 本题考查了电解原理,为高频考点,根据N元素化合价变化确定阴阳极、正负极,难点是电极反应式的书写,注意氢离子还进入阴极室,很多同学往往只考虑析出的气体而导致错误,为易错点.

练习册系列答案
相关题目
18.下列各组离子或分子能大量共存,当加入相应试剂后,发生反应的离子方程式书写正确的是( )
| 选项 | 离子组 | 加入试剂 | 加入试剂后发生反应的离子方程式 |
| A | NH4+、Fe2+、SO42- | 少量Ba(OH)2溶液 | 2NH4++SO42-+Ba2++2OH-=BaSO4↓+2NH3•H2O |
| B | Na+、OH-、Cl- | 少量Mg(HCO3)2溶液 | Mg2++2HCO3-+4OH-=2H2O+Mg(OH)2↓+2CO32- |
| C | K+、NH3•H2O、CO32- | 通入少量CO2 | 2OH-+CO2=CO32-+H2O |
| D | Fe2+、NO3-、HSO3- | NaHSO4溶液 | HSO3-+H+=SO2↑+H2O |
| A. | A | B. | B | C. | C | D. | D |
19.X、Y、Z均为短周期元素,原子序数依次增大,X3+比Z2-少一个电子层.以下说法不正确的是( )
| A. | 原子半径:X>Y>Z | B. | 氧化物的熔点:Z>X | ||
| C. | 简单氢化物稳定性:Z>Y | D. | X、Y、Z单质的晶体类型可能有三种 |
16.某有机物的结构简式如图所示,下列有关该有机物的说法正确的是( )


| A. | 分子中含有四种官能团 | |
| B. | 1mol该有机物完全燃烧消耗O2的物质的量为10mol | |
| C. | 能发生加成、取代、消去、水解等反应 | |
| D. | 相同条件下,等量的该有机物分别与足量的Na和NaHCO3溶液反应产生的气体的量相同 |
3.化学与人类的生活、生产息息相关,下列说法正确的是( )
| A. | BaSO4在医学上用作“钡餐”,Ba2+对人体无害 | |
| B. | 高锰酸钾溶液、酒精、双氧水都能杀菌消毒,消毒原理相同,都利用了强氧化性 | |
| C. | 光导纤维的主要成分是单质硅,太阳能电池使用的材料是SiO2 | |
| D. | “地沟油”禁止食用,但可以用来制肥皂或燃油 |
20.下列说法中不正确的是( )
| A. | 宇宙星体、地球内部都处于高压状态,探究“高压下钠和锂单质金属→绝缘体转变”现象的本质、理解处于高压状态下一些物质的行为具有重要意义,它们可以为研究星体和地球内部构造提供理论支持 | |
| B. | 工业、农业以及日常生活中产生的污水应当分开处理.常用的污水处理方法有中和法、氧化还原法、离子交换法、萃取法、吹脱法、吸附法、电渗析法等,其中前三种属于化学处理方法 | |
| C. | 新型炸药--C4塑胶炸药得名于其空间网状延展结构的每个结构基元含有4个碳原子,由于该炸药成体时无需包裹金属外壳及添加金属芯件,因此能轻易躲过普通X光安全检查,具有较强的隐蔽性 | |
| D. | 建筑领域常使用的黏土、石英、白垩石和多用于农业和食品工业的硅藻土、硅胶均不属于硅酸盐材料的范畴 |
17.有a、b、c、d四种元素,均为原子序数依次增大的前20号元素.a存在a+和a-两种 离子,b和c为同一主族元素,c的次外层有8个电子,c2-和d2+的电子层结构相同.下列叙述正确的是( )
| A. | b、c与a形成化合物的稳定性一定为c>b | |
| B. | a和d形成的化合物与水反应产生气体可以作燃料 | |
| C. | c、a和b可形成的化合物为离子化合物 | |
| D. | a、b、c、d四种元素组成的化合物的水溶液可以为酸性、也可以为碱性 |
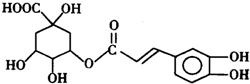 .
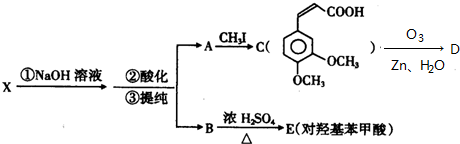
.
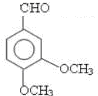 ;
;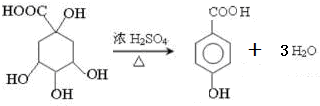 ;
;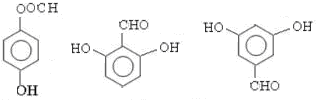 任意一种;(任写一种)
任意一种;(任写一种)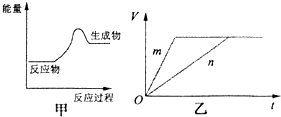 现有反应:A.CaCO3═CaO+CO2
现有反应:A.CaCO3═CaO+CO2