题目内容
6.“绿色试剂”双氧水可作为矿业废液消毒剂,如消除采矿业废液中的氰化物(如KCN),化学方程为:KCN+H2O2+H2O→A+NH3↑(已知配平)
(1)生成物A是一种盐,它的化学式为KHCO3;
(2)用单线桥表示该反应电子转移的方向和数目:
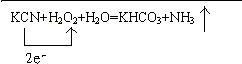 .
.
分析 (1)质量守恒定律来分析A的化学式;
(2)化合价的变化来计算转移的电子数,失电子一方指向得到电子的一方.
解答 解:(1)KCN+H2O2+H2O→A+NH3↑,由质量守恒定律可知,反应前后的元素守恒、原子个数守恒,则A的化学式为KHCO3,故答案为:KHCO3;
(2)KCN+H2O2+H2O=KHCO3+NH3↑中转移2个电子,所以单线桥表示出该反应电子转移的方向和数目为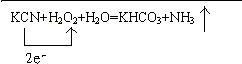 ,
,
故答案为: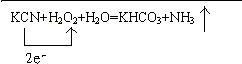 .
.
点评 本题考查氧化还原反应的计算,明确氧化还原反应中的元素的化合价变化及氧化还原反应中的基本概念即可解答,注意物质的量与转移电子数的关系,题目难度不大.

练习册系列答案
相关题目
1.下列化学式既能表示物质的组成,又能表示物质的一个分子的是( )
| A. | NH3 | B. | NaOH | C. | SiO2 | D. | Fe |
11.下列各组物质按酸、碱、盐、氧化物顺序分类正确的是( )
| A. | 硫酸、纯碱、石膏、铁红 | B. | 醋酸、烧碱、纯碱、生石灰 | ||
| C. | 碳酸、熟石膏、小苏打、三氧化硫 | D. | 氯化氢、苛性钠、氯化钠、石灰石 |
15.分类方法在化学学科的发展中起着非常重要的作用.下列分类标准合理的是( )
| A. | 根据物质能否导电将物质分为电解质和非电解质 | |
| B. | 根据反应中的热效应将化学反应分为放热反应和吸热反应 | |
| C. | 根据溶液导电性强弱将电解质分为强电解质和弱非电解质 | |
| D. | 根据元素的化合价的高低将化学反应分为氧化还原反应和非氧化还原反应 |
17.根据下列能量变化示意图,分析下列说法中正确的是( )


| A. | A(g)+B(g)→C(g)+D(l)是放热反应 | |
| B. | A(g)+B(g)→C(g)+D(l)是吸热反应 | |
| C. | C(g)+D(l)→A(g)+B(g)是放热反应 | |
| D. | C(g)+D(l)具有的能量大于A(g)+B(g)具有的能量 |
 ,氧化产物是K2SO3,氧化剂与还原剂的物质的量之比为2:1,若反应中消耗了0.6molS,则反应中转移的电子为0.8mol.
,氧化产物是K2SO3,氧化剂与还原剂的物质的量之比为2:1,若反应中消耗了0.6molS,则反应中转移的电子为0.8mol.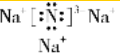 ,该化合物是由离子键形成的.
,该化合物是由离子键形成的.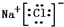 、
、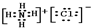 .
.