题目内容
2.5molBa(OH)2中含有 个Ba2+,含有 个OH-;5molNa2SO4溶于水电离出Na+ 个;0.6mol的Al2(SO4)3 中含Al3+ mol.
考点:物质的量的相关计算
专题:
分析:钡离子物质的量等于氢氧化钡物质的量,氢氧根离子物质的量等于氢氧化钡的2倍,根据N=nNA计算Ba2+、OH-离子数目;
硫酸钠电离出的钠离子物质的量为硫酸钠的2倍,根据N=nNA计算Na+离子数目;
铝离子物质的量为硫酸铝的2倍.
硫酸钠电离出的钠离子物质的量为硫酸钠的2倍,根据N=nNA计算Na+离子数目;
铝离子物质的量为硫酸铝的2倍.
解答:
解:n(Ba2+)=n[Ba(OH)2]=2.5mol,故Ba2+离子数目为2.5mol×NAmol-1=2.5NA,n(OH-)=2n[Ba(OH)2]=5mol,故OH-离子数目为5mol×NAmol-1=5NA;
n(Na+)=n(Na2SO4)=10mol,故Na+离子数目为10mol×NAmol-1=10NA;
n(Al3+)=n[Al2(SO4)3]=0.6mol×2=1.2mol,
故答案为:2.5NA;5NA;10NA;1.2.
n(Na+)=n(Na2SO4)=10mol,故Na+离子数目为10mol×NAmol-1=10NA;
n(Al3+)=n[Al2(SO4)3]=0.6mol×2=1.2mol,
故答案为:2.5NA;5NA;10NA;1.2.
点评:本题考查微粒数目的计算,难度不大,注意对化学式的理解.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列过程或现象与水解无关的是( )
| A、纯碱溶液去油污 |
| B、配制氯化铁溶液时加入少量的盐酸 |
| C、NaHCO3与Al2(SO4)3混合作泡沫灭火剂 |
| D、铁在潮湿的环境下生锈 |
下列说法正确的是( )
| A、CO(g)的燃烧热:△H=-283.0kJ/mol,则2CO2(g)=2CO(g)+O2(g)反应的△H=+566.0kJ/mol |
| B、已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.3 kJ?mol-1,则含40.0g NaOH的稀溶液与稀醋酸完全中和,放出57.3kJ的热量 |
| C、己知2C(s)+2O2(g)=2CO2(g)△H=a;2C(s)+O2(g)=2CO(g);△H=b,则a>b |
| D、已知C (石墨,s)=C (金刚石,s)△H>0,则石墨比金刚石稳定 |
下列关于浓HNO3和浓H2SO4的叙述中正确的是( )
| A、常温下都可用铝制容器贮存 |
| B、露置在空气中,容器内酸液的质量都减轻 |
| C、常温下都能与铜较快反应 |
| D、露置在空气中,容器内酸液的浓度都增大 |
下列实验现象,与新制氯水中的某些成分(括号内物质)没有关系的是( )
| A、向干燥红色布条中滴加新制氯水,红色布条会褪色(HCl) |
| B、向NaHCO3固体中加入新制氯水,有无色气泡产生(H+) |
| C、将AgNO3溶液滴加到新制氯水中,有白色沉淀产生(Cl-) |
| D、向FeCl2溶液中滴加新制氯水,再滴加KSCN溶液,溶液呈红色(Cl2) |
如图是关于N2+3H2?2NH3△H<0的速率-时间图象,则t1时刻使平衡发生移动的原因是( )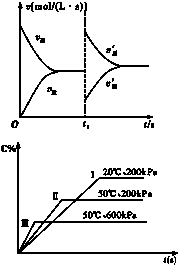

| A、升高温度,同时增大压强 |
| B、降低温度,同时减小压强 |
| C、增大反应物的浓度,同时使用适宜的催化剂 |
| D、增大反应物的浓度,同时减小生成物的浓度 |
 已知一定温度和压强下,在容积为VL的密闭容器中充入1molA和1molB,保持恒温恒压下反应:A(g)+B(g)?C(g)△H<0.达到平衡时,C的体积分数为40%.试回答有关问题:
已知一定温度和压强下,在容积为VL的密闭容器中充入1molA和1molB,保持恒温恒压下反应:A(g)+B(g)?C(g)△H<0.达到平衡时,C的体积分数为40%.试回答有关问题: