题目内容
如图是关于N2+3H2?2NH3△H<0的速率-时间图象,则t1时刻使平衡发生移动的原因是( )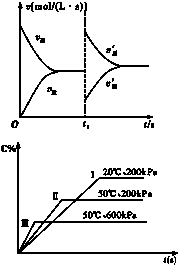

| A、升高温度,同时增大压强 |
| B、降低温度,同时减小压强 |
| C、增大反应物的浓度,同时使用适宜的催化剂 |
| D、增大反应物的浓度,同时减小生成物的浓度 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:由图可知在t1时,正反应速率突然变大,逆速率突然减小,结合外界条件对反应速率的影响,综合分析解答.
解答:
解:A、升高温度,同时增大压强,正逆反应速率都应在原平衡点的上方,故A错误;
B、降低温度,同时减小压强,正逆反应速率都应在原平衡点的下方,故B错误;
C、增大反应物的浓度,同时使用适宜的催化剂,正逆反应速率都应在原平衡点的上方,故C错误;
D、增大反应物的浓度,正反应速率变大在原平衡点的上方,同时减小生成物的浓度,逆反应速率降低在原平衡点的下方,故D正确;
故选:D.
B、降低温度,同时减小压强,正逆反应速率都应在原平衡点的下方,故B错误;
C、增大反应物的浓度,同时使用适宜的催化剂,正逆反应速率都应在原平衡点的上方,故C错误;
D、增大反应物的浓度,正反应速率变大在原平衡点的上方,同时减小生成物的浓度,逆反应速率降低在原平衡点的下方,故D正确;
故选:D.
点评:本题图象分析题,考查时结合外界条件对化学反应速率的影响,学生在解题时应抓住特殊点,就能迅速解题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
价电子排布为5s25p1的元素,在周期表中的位置是( )
| A、第四周期第ⅤA族 |
| B、第五周期第ⅢA族 |
| C、第五周期第ⅠA族 |
| D、第四周期第ⅢA族 |
用NA表示阿伏伽德罗常熟的值.下列说法正确的是( )
| A、标准状况下,22.4LH2O中含有的分子数为NA |
| B、常温常压下,32gO2中含有的分子数为NA |
| C、1molMg与足量N2反应时转移的电子数为NA |
| D、1L1mol?L-1CaCl2溶液中含有的氯离子数为NA |
分类是化学学习和研究的常用方法.下列分类依据和结论都正确的是( )
| A、溶液、胶体、浊液均为分散系,都属于混合物 |
| B、H2SO4、NaOH、NaC1均为强电解质,都属于离子化合物 |
| C、Al、Al2O3、Al(OH)3均能与盐酸反应又能与氢氧化钠溶液反应,都是具两性的化合物 |
| D、H2O、CH3COOH、Cu2(OH)2CO3均含有氧元素,都是氧化物 |
对于在一密闭容器中进行的下列反应:C(s)+O2(g)?CO2(g)下列说法中错误的是( )
| A、将木炭粉碎成粉末状可以加快化学反应速率 |
| B、升高温度可以加快化学反应速率 |
| C、增加压强不能加快化学反应速率 |
| D、增加木炭的量可以加快化学反应速率 |
有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份100mL溶液进行如下实验:(1)第一份加入AgNO3溶液有沉淀产生.(2)第二份加足量NaOH溶液加热后,收集到气体0.04mol(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g.根据上述实验,以下推测错误的是( )
| A、K+一定存在 |
| B、每份取样溶液中含0.02mol CO32- |
| C、Cl-可能存在 |
| D、Ba2+一定不存在,Mg2+可能存在 |
常温下将pH=2的盐酸和pH=11的氢氧化钠溶液,以体积比1:9混合后,溶液的pH是( )
| A、3 | B、4 | C、9 | D、10 |
