题目内容
17.将一定量的Cl2通入30mL10.00 mol•L-1的浓KOH溶液中,适当加热使溶液中形成KCl、KClO、KClO3共存体系,下列有关说法错误的是 ( )| A. | 溶液中n(KCl)=n(KClO)+5n(KClO3) | |
| B. | 参加反应的氯气的物质的量一定为0.15mol | |
| C. | 若反应中转移电子为nmol,则0.15mol<n<0.25mol | |
| D. | 共存体系溶液中,n(K+)、n(Cl-)可能为7:3 |
分析 形成KCl、KClO、KClO3共存体系,Cl元素的化合价由0降低为-1价,Cl元素的化合价由0升高为+1、+5价,Cl2既是氧化剂又是还原剂,结合原子守恒及电子守恒解答.
解答 解:A.由电子守恒可知,n(KCl)×(1-0)=n(KClO)×(1-0)+n(KClO3)×(5-0),则溶液中存在n(KCl)=n(KClO)+5n(KClO3),故A正确;
B.KCl、KClO、KClO3共存体系中K、Cl的原子个数相同,由原子守恒可知,参加反应的氯气的物质的量一定为0.03L×10mol/L×$\frac{1}{2}$=0.15mol,故B正确;
C.由K原子守恒可知若生成等物质的量的KCl、KClO,转移电子为0.15mol,若生成KCl、KClO3,二者物质的量比为5:1,转移电子为0.3mol×$\frac{1}{6}$×(5-0)=0.25mol,适当加热使溶液中形成KCl、KClO、KClO3共存体系,则反应中转移电子为nmol,可知0.15mol<n<0.25mol,故C正确;
D.KCl、KClO、KClO3共存体系中,KCl电离出Cl-,n(K+)、n(Cl-)为7:3,若7molK+,则生成KCl为3mol,得到电子为3mol,若只生成KClO失去电子为4mol,若只生成KClO3失去为4mol×5=20mol,一定不遵循电子守恒,故D错误;
故选D.
点评 本题考查氧化还原反应的计算,为高频考点,把握反应中元素的化合价变化、电子和原子守恒为解答的关键,侧重分析与计算能力的考查,题目难度中等.

练习册系列答案
相关题目
8.表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是:Ne(填具体元素符号);非金属性最强的元素是F(填具体元素符号),原子结构示意图为 .元素⑩名称为溴.
.元素⑩名称为溴.
(2)在这些元素最高价氧化物对应的水化物中,酸性最强是HClO4(填化学式)
(3)⑦的单质能与NaOH溶液反应,离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑
(4)在这些元素中,最高价氧化物对应的水化物能与其气态氢化物化合生成盐的元素是②(填编号)
(5)⑥⑦⑧⑨四种元素对应的简单离子中,离子半径最小的是Al3+(填离子符号)
(6)⑧和⑨都是重要的非金属元素.下列叙述中,能说明⑨的非金属性比⑧强的是bc
a.氢化物的沸点:⑨>⑧
b.⑨的单质与氢气化合比⑧的单质容易
c.⑨的单质可置换出⑧的单质
d.⑨的氢化物的酸性比⑧的氢化物的酸性强.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | ④ | ⑤ | |||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ||||
| 4 | ⑩ |
 .元素⑩名称为溴.
.元素⑩名称为溴.(2)在这些元素最高价氧化物对应的水化物中,酸性最强是HClO4(填化学式)
(3)⑦的单质能与NaOH溶液反应,离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑
(4)在这些元素中,最高价氧化物对应的水化物能与其气态氢化物化合生成盐的元素是②(填编号)
(5)⑥⑦⑧⑨四种元素对应的简单离子中,离子半径最小的是Al3+(填离子符号)
(6)⑧和⑨都是重要的非金属元素.下列叙述中,能说明⑨的非金属性比⑧强的是bc
a.氢化物的沸点:⑨>⑧
b.⑨的单质与氢气化合比⑧的单质容易
c.⑨的单质可置换出⑧的单质
d.⑨的氢化物的酸性比⑧的氢化物的酸性强.
5.汽车在剧烈碰撞时,安全气囊中发生反应:10NaN3+2KNO3=K2O+5Na2O+16N2↑,下列关于该反应的说法正确的是( )
| A. | 22.4LN2中σ键与π键个数比为1:2 | |
| B. | 反应物和生成物中只有氮气属于非电解质 | |
| C. | 该反应每转移1mol电子,有0.2molKNO3被氧化 | |
| D. | NaN3是只含离子键的离子化合物 |
12. 25℃时向20mL0.1 mol•L-1醋酸溶液中不断滴入0.1
25℃时向20mL0.1 mol•L-1醋酸溶液中不断滴入0.1
mol•L-1NaOH溶液,溶液pH变化如图所示.此过程中
下列说法正确的是(溶液混合忽略体积变化)( )
 25℃时向20mL0.1 mol•L-1醋酸溶液中不断滴入0.1
25℃时向20mL0.1 mol•L-1醋酸溶液中不断滴入0.1 mol•L-1NaOH溶液,溶液pH变化如图所示.此过程中
下列说法正确的是(溶液混合忽略体积变化)( )
| A. | a点:c(CH3COO-)<c(Na+) | |
| B. | 水的电离程度:c点小于d点 | |
| C. | b点时,NaoH和CH3COOH恰好完全反应 | |
| D. | d点:c(OH-)-c(H+)+c(CH3COOH)=0.2 mol•L-1 |
2.下列关于硅原子的核外电子排布表示式(或排布图)中,错误的是( )
| A. | 1s22s22p63s23p2 | B. | [Ne]3s23p2 | ||
| C. | 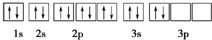 | D. |  |
9.下列物质分子中,既含有极性键又含有非极性键的非极性分子是( )
| A. | C2H4 | B. | Br2 | C. | Na2O2 | D. | CH3COOH |
7.形成节约能源和保护生态环境的产业结构是人类与自然和谐发展的重要保证,你认为下列行为中有悖于这一保证的是( )
| A. | 开发太阳能、水能、风能等新能源,减少使用煤、石油等化石燃料 | |
| B. | 研究采煤、采油新技术,提高产量以满足工业生产的快速发展 | |
| C. | 在农村推广使用沼气 | |
| D. | 减少资源消耗、增加资源的重复使用和资源的循环再生 |
