题目内容
20.化合物HIn在水溶液中因存在以下电离平衡,故可用作酸碱指示剂: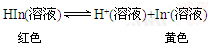
浓度为0.02mol/L的下列各溶液:①盐酸②石灰水③NaCl溶液④氨水⑤NaHCO3溶液⑥NaHSO4溶液 其中能使指示剂显红色的是( )
| A. | ①④⑤ | B. | ②⑤⑥ | C. | ③④ | D. | ①⑥ |
分析 能使指示剂显红色,应使c(HIn)>c(In-),所加入物质应使平衡向逆反应方向移动,所加入溶液应呈酸性,以此解答该题.
解答 解:能使指示剂显红色,应使c(HIn)>c(In-),所加入物质应使平衡向逆反应方向移动,所加入溶液应呈酸性,①⑥为酸性溶液,可使平衡向逆反应方向移动,而②④⑤溶液呈碱性,可使平衡向正反应方向移动,③为中性溶液,平衡不移动,
故选D.
点评 本题考查化学平衡的影响因素,题目难度不大,注意根据颜色的变化判断平衡移动的移动方向,结合外界条件对平衡移动的影响分析.

练习册系列答案
相关题目
6. 如图,在盛有稀硫酸的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是( )
如图,在盛有稀硫酸的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是( )
 如图,在盛有稀硫酸的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是( )
如图,在盛有稀硫酸的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是( )| A. | 外电路的电流方向为X→外电路→Y | |
| B. | 若两电极都是金属,则它们的活动性顺序为X<Y | |
| C. | X极上发生的是还原反应,Y极上发生的是氧化反应 | |
| D. | SO42-向X电极移动 |
11.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | 通入足量CO2后的溶液中:Na+、SiO32-、CH3COO-、SO32- | |
| B. | 饱和氯水中:Cl-、NO3-、Na+、SO32- | |
| C. | c(H+)=1×10-1 mol•L-1的溶液中:Cu2+、Al3+、SO42-、NO3- | |
| D. | 0.1 mol•L-1 CH3COONa溶液:H+、Al3+、Cl-、NO3- |
15.航天科学技术测得,三氧化二碳(C2O3)是金星大气层的成分之一.下列说法正确的是( )
| A. | C2O3和CO2是同素异形体 | B. | C2O3和CO完全燃烧,产物都是CO2 | ||
| C. | C2O3和CO都是酸性氧化物 | D. | C2O3和CO2互为同分异构体 |
5.在相同温度时,100mL 0.01mol•L-1的醋酸溶液与10mL 0.1mol•L-1的醋酸溶液相比较,下列数据中,前者大于后者的是( )
①H+的物质的量 ②电离程度 ③中和时所需氢氧化钠溶液的量 ④醋酸的物质的量.
①H+的物质的量 ②电离程度 ③中和时所需氢氧化钠溶液的量 ④醋酸的物质的量.
| A. | ①② | B. | ②③ | C. | ①④ | D. | ②④ |
12.W、X、Y、Z、Q是五种常见的短周期主族元素,原子序数依次增大,在周期表中W原子半径最小;X元素原子核外电子总数是其次外层电子数的3倍;W和Y、X和Z均位于同一主族;Q的非金属性在同周期元素中最强.下列说法正确的是( )
| A. | 简单离子半径:Y>Q | |
| B. | Q分别与X、Z形成的最简单化合物中化学键类型相同 | |
| C. | YW能与WQ发生复分解反应 | |
| D. | 最简单气态氢化物的稳定性:X<Z |
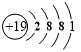 .
.
 如图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物,已知:
如图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物,已知: