题目内容
5.在相同温度时,100mL 0.01mol•L-1的醋酸溶液与10mL 0.1mol•L-1的醋酸溶液相比较,下列数据中,前者大于后者的是( )①H+的物质的量 ②电离程度 ③中和时所需氢氧化钠溶液的量 ④醋酸的物质的量.
| A. | ①② | B. | ②③ | C. | ①④ | D. | ②④ |
分析 在相同温度时,100mL 0.01mol•L-1的醋酸溶液与10mL0.1mol•L-1的醋酸溶液中溶质都为0.001mol,醋酸为弱电解质,浓度不同,电离程度不同,浓度越大,电离程度越小,以此解答该题.
解答 解:①醋酸为弱电解质,浓度越大,电离程度越小,两种溶液溶质都为0.001mol,则100mL 0.01mol•L-1的醋酸溶液与10mL0.1mol•L-1的醋酸溶液相比较,H+的物质的量前者大,故①正确;
②醋酸为弱电解质,浓度越大,电离程度越小,电离程度0.01mol•L-1的醋酸大,故②正确;
③由于溶质n(CH3COOH)都为0.001mol,中和时所需NaOH的量应相同,故③错误;
④0.01mol•L-1的醋酸电离程度大,则溶液中CH3COOH分子的物质的量小,故④错误;
故选A.
点评 本题考查弱电解质的电离,题目难度不大,注意醋酸为弱电解质,醋酸的浓度不同,电离程度不同,浓度越大,电离程度越小的特征,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
11.化学是一门实用性强的自然科学,在社会、生产、生活中起着重要的作用,下列说法不正确的是( )
| A. | 油条的制作口诀是“一碱、二矾、三钱盐”,其中的“碱”是烧碱 | |
| B. | 黑火药的最优化配方是“一硫二硝三木炭”,其中的“硝”是硝酸钾 | |
| C. | 过滤操作要领是“一贴二低三靠”,其中“贴”是指滤纸紧贴漏斗的内壁 | |
| D. | “固体需匙或纸槽,一送二竖三弹弹;块固还是镊子好,一横二放三慢竖“.前一个固体一般指粉末状固体 |
13.与水一样,甲醇也能微弱电离:2CH3OH(l)?CH3OH2++CH3O-,25℃时,K=2.0×10-17.若甲醇中加入少量金属钠,则下列叙述不正确的是( )
| A. | 金属钠与水反应比金属钠与甲醇反应更剧烈 | |
| B. | 结合H+的能力CH3O-<OH- | |
| C. | 所得到溶液中K=c(CH3O-)×c(CH3OH2+) | |
| D. | 所得到溶液中c(Na+)+c(CH3OH2+)═c(CH3O-) |
20.化合物HIn在水溶液中因存在以下电离平衡,故可用作酸碱指示剂: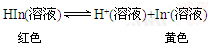
浓度为0.02mol/L的下列各溶液:①盐酸②石灰水③NaCl溶液④氨水⑤NaHCO3溶液⑥NaHSO4溶液 其中能使指示剂显红色的是( )
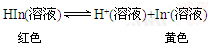
浓度为0.02mol/L的下列各溶液:①盐酸②石灰水③NaCl溶液④氨水⑤NaHCO3溶液⑥NaHSO4溶液 其中能使指示剂显红色的是( )
| A. | ①④⑤ | B. | ②⑤⑥ | C. | ③④ | D. | ①⑥ |
10.下列各项中的两个量,其比值一定为2:1的是( )
| A. | 在相同温度下,等浓度的H2SO4和CH3COOH溶液中的c(H+) | |
| B. | 相同温度下,等浓度的Ba(OH)2和NaOH溶液,前者与后者的c(OH-) | |
| C. | 相同温度下,0.2 mol•L-1醋酸溶液和0.1 mol•L-1醋酸溶液中的c(H+) | |
| D. | 液面在“0”刻度时,50 mL碱式滴定管和25 mL碱式滴定管所盛液体的体积 |
14.下列各组物质按酸、碱、盐分类顺序排列正确的是( )
| A. | 硫酸、纯碱、食盐 | B. | 醋酸、烧碱、生石灰 | ||
| C. | 硝酸、烧碱、胆矾 | D. | 盐酸、熟石灰、氧化镁 |
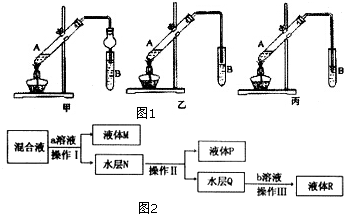
 .
.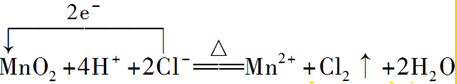 .
. .
.