题目内容
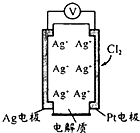 利用如图所示原电池可测量空气中Cl2含量,其中电解质是Ag+可以自由移动的固体
利用如图所示原电池可测量空气中Cl2含量,其中电解质是Ag+可以自由移动的固体物质.下列分析不正确的是( )
| A、电子经外电路流向Pt电极 |
| B、电池工作时,电解质中Ag+数目减少 |
| C、正极反应:C12+2e-+2Ag+=2AgCl |
| D、空气中c(C12)越大,Ag极消耗速率越快 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:Ag电极为负极发生氧化反应生成银离子,氯气在正极发生还原反应生成氯离子,氯离子与银离子反应生成AgCl沉淀,据沉淀质量测定氯气含量,据此分析.
解答:
解:A、电子从负极流向正极Pt,故A正确;
B、电池工作时,电解质中Ag+数目不变,故B错误;
C、氯气在正极发生还原反应生成氯离子,氯离子与银离子反应生成AgCl沉淀,故C正确;
D、反应原理是Ag与氯气反应,故D正确;
故选B.
B、电池工作时,电解质中Ag+数目不变,故B错误;
C、氯气在正极发生还原反应生成氯离子,氯离子与银离子反应生成AgCl沉淀,故C正确;
D、反应原理是Ag与氯气反应,故D正确;
故选B.
点评:本题考查了原电池原理的应用,注意电解反应类型和电子移动方向,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
与水一样,甲醇也能微弱电离:2CH3OH(l)═CH3OH2++CH3O-,25℃时,K=2.0×10-17.若往一定量的甲醇中加入金属钠,则有关叙述正确的是( )
| A、金属钠与甲醇反应比金属钠与水反应更剧烈 |
| B、结合H+的能力CH3O->OH- |
| C、所得到溶液中K=c(CH3O-)×c(CH3OH2+) |
| D、所得到溶液中c(Na+)=c(CH3OH2+)+c(CH3O-) |
下列物质中,不属于电解质的是( )
| A、NaCl |
| B、KOH |
| C、H2SO4 |
| D、CH3CH2OH |
下列晶体模型对应的物质熔化时破坏共价键的是( )
A、 金刚石模型 金刚石模型 |
B、 干冰模型 |
C、 碳60模型 |
D、 氯化钠模型 |
有关化学用语表达,下列正确的是( )
A、CS2的比例模型: |
B、铍原子最外层的电子云图: |
| C、石英的分子式:SiO2 |
D、氮原子最外层轨道表示式: |
下列有关说法错误的是( )
| A、常用丁达尔效区分溶液与胶体 |
| B、在铜锌原电池中,负极上发生Zn-2e-═Zn2+ |
| C、常温下,稀释0.1 mol/L的氨水,溶液中c(OH-)、c(NH4+)、c(H+)均减少 |
| D、向AgCl沉淀中滴加KI溶液,沉淀变为黄色,说明Ksp(AgCl)>Ksp(AgI) |