题目内容
8.在一个1L的密闭容器中,加入2molA和1molB,发生下述反应:2A(g)+B(g)?3C(g)+D(s),达到平衡时,C的浓度为1.2mol/L.若维持容器的体积和温度不变,只加入C和D作为起始物质,使反应从逆反应开始,达到平衡时,C的浓度仍是1.2mol/L,则D的起始物质的量应满足的条件是( )| A. | 大于零即可 | B. | 大于0.6mol | C. | 大于或等于1mol | D. | 任意值 |
分析 在恒温恒容条件下,C的浓度仍为1.2mol/L,假设反应完全逆向,则在折算之后要满足n(A)=2mol,n(B)=1mol,D为固体,对平衡移动没有影响,据此分析.
解答 解:在恒温恒容条件下,C的浓度仍为1.2mol/L,假设反应完全逆向,则在折算之后要满足n(A)=2mol,n(B)=1mol,所以加入的C和D分别为3mol和1mol,但又D为固体,对平衡移动没有影响,所以D只要能够与C反应达到平衡状态的量即可,所以D最少为$\frac{3-1.2}{3}$=0.6mol,所以B正确;
故选B.
点评 考查化学平衡的有关计算、等效平衡,难度中等,构建平衡建立的途径是解题关键,注意等效平衡规律:
1、恒温恒压下,按化学计量数转化到一边,满足对应物质的物质的量之比相同,为等效平衡;
2、恒温恒容下,若反应前后气体气体发生变化,按化学计量数转化到一边,满足对应物质的物质的量相等,为等效平衡;若反应前后气体的体积不变,按化学计量数转化到一边,满足对应物质的物质的量之比相同,为等效平衡

练习册系列答案
 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案
相关题目
20.阿伏加德罗常数为NA,下列说法正确的是( )
| A. | 1mol钠与氧气反应生成Na2O或Na2O2时,失电子数目均为NA | |
| B. | 将含有0.1molFeCl3的饱和溶液滴入沸水中,产生胶粒的数目为0.1NA | |
| C. | 1molC7H16中含有共价键的数目为23NA | |
| D. | 常温下,1L 0.1 mol•L-1的Na2CO3溶液中含有的离子总数为0.3NA |
17.某同学用下列装置(固定、加热仪器和橡胶管略)进行有关氨气制取的实验探究,回答下列问题.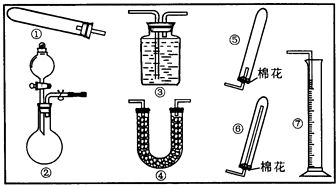
(1)若用装置①制取NH3,其反应的化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑;
若要测定生成的NH3的体积,则必须选择的装置是③⑦(填装置序号),装置中所盛试剂应具有的性质是氨气和该液体不能反应、氨气不能溶于该液体、该液体不能挥发.
(2)若用装置②制取并收集干燥的NH3,烧瓶内装的试剂是CaO或(NaOH或碱石灰),分液漏斗中装的试剂是浓氨水(或浓NH4Cl溶液),收集装置应选择⑥(填装置序号).
证明氨气已收集满的操作是用湿润的红色石蕊试纸靠近管口,若试纸变蓝则证明已收集满
检验装置②的气密性的方法是在橡胶管处接上导气管,关闭分液漏斗活塞,打开止水夹,将导气管末端插入水槽中,用热毛巾捂着烧瓶(或用酒精灯微热),导气管末端有气泡冒出,移开热毛巾(或停止加热)一段时间,导气管末端有一段水柱(或关闭装置②的止水夹和分液漏斗活塞,从分液漏斗的上端注入一定量的水,打开分液漏斗活塞,若漏斗中的水滴入烧瓶中的速率逐渐减慢至不再滴入,说明装置气密性良好)
(3)若用下列各种试剂组合(其它条件相同)进行制取氨气的对比实验,测出氨气的体积
(标准状况)如下表:
从表中数据分析,实验室制氨气的产率最高的⑥其原因是因为NH4Cl受热易分解,生成的部分NH3和HCl又重新结合生成NH4Cl;而用Ca(OH)2反应产生的水较多,吸收的NH3较多,所以用CaO和(NH4)2SO4反应产率最高.

(1)若用装置①制取NH3,其反应的化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑;
若要测定生成的NH3的体积,则必须选择的装置是③⑦(填装置序号),装置中所盛试剂应具有的性质是氨气和该液体不能反应、氨气不能溶于该液体、该液体不能挥发.
(2)若用装置②制取并收集干燥的NH3,烧瓶内装的试剂是CaO或(NaOH或碱石灰),分液漏斗中装的试剂是浓氨水(或浓NH4Cl溶液),收集装置应选择⑥(填装置序号).
证明氨气已收集满的操作是用湿润的红色石蕊试纸靠近管口,若试纸变蓝则证明已收集满
检验装置②的气密性的方法是在橡胶管处接上导气管,关闭分液漏斗活塞,打开止水夹,将导气管末端插入水槽中,用热毛巾捂着烧瓶(或用酒精灯微热),导气管末端有气泡冒出,移开热毛巾(或停止加热)一段时间,导气管末端有一段水柱(或关闭装置②的止水夹和分液漏斗活塞,从分液漏斗的上端注入一定量的水,打开分液漏斗活塞,若漏斗中的水滴入烧瓶中的速率逐渐减慢至不再滴入,说明装置气密性良好)
(3)若用下列各种试剂组合(其它条件相同)进行制取氨气的对比实验,测出氨气的体积
(标准状况)如下表:
| 试剂组合/NH3体积(mL) | 6.0gCa(OH)2(s,过量) | 6.0NaOH(s,过量) | 6.0g CaO(s,过量) |
| 5.4g NH4Cl(s) | ①/1344 | ②/1568 | ③/1792 |
| 5.4(NH4)2SO4(s) | ④1364 | ⑤1559 | ⑥/1753 |
12.下列物质中碱性最强的是( )
| A. | LiOH | B. | NaOH | C. | Mg(OH)2 | D. | Al(OH)3 |
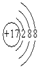

 ,化合物中含有离子键键(填离子或共价)
,化合物中含有离子键键(填离子或共价)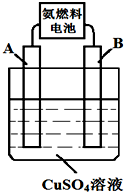 能源的开发、利用与人类社会的可持续发展息息相关,怎样充分利用好能源是摆在人类面前的重大课题.
能源的开发、利用与人类社会的可持续发展息息相关,怎样充分利用好能源是摆在人类面前的重大课题.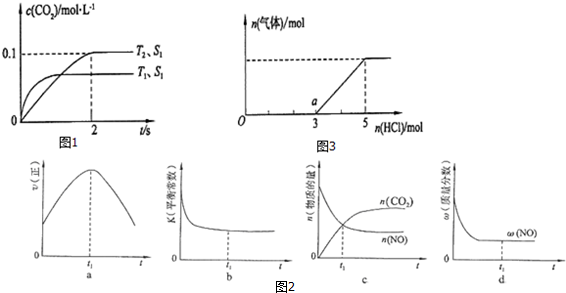

 .
. .
.