题目内容
18.A、B、C、D四种短周期元素,0.5molA元素的离子得到NA个电子后被还原为中性原子;0.4g A的氧化物恰好与100mL0.2moL/L的盐酸完全反应;A元素原子核内质子数和中子数相等.B元素原子核外电子数比A元素原子核外电子数多1;C-离子核外电子层数比A元素的离子核外电子层数多1;D元素的原子最外层电子数是次外层电子数的2倍.填写下列空格:(1)推断A、B、C、D四种元素(写出元素的名称)A镁B铝
(2)C的一价阴离子的结构示意图
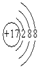
(3)D元素的最高价氧化物的电子式是

(4)用电子式表示A、C两元素组成化合物的形成过程
 ,化合物中含有离子键键(填离子或共价)
,化合物中含有离子键键(填离子或共价)(5)写出B单质与NaOH溶液反应的离子方程式2Al+2OH-+2H2O=2AlO2-+3H2↑.
分析 短周期元素A、B、C、D中,0.5mol A元素的离子得到NA个电子被还原为中性原子,则A离子带两个单位正电荷,0.4g A的氧化物恰好与100ml 0.2mol/L的盐酸完全反应,HCl的物质的量=0.1L×0.2mol/L=0.02mol,由AO+2HCl═ACl2+H2O,可知0.4gAO的物质的量为0.01mol,则M(AO)=0.4g0.01mol=40g/mol,故A的摩尔质量为40g/mol-16g/mol=24g/mol,A原子核内质子数目与中子数目相等,则质子数为12,即A为Mg元素;B元素原子核外电子数比A元素原子核外电子数多1,则B为Al;C-比A元素的离子多1个电子层,则C的质子数为18-1=17,即C为Cl元素;D元素原子最外层电子数是次外层电子数的2倍,原子只能有2个电子层,最外层电子数为4,即D为C元素,以此解答.
解答 解:短周期元素A、B、C、D中,0.5mol A元素的离子得到NA个电子被还原为中性原子,则A离子带两个单位正电荷,0.4g A的氧化物恰好与100ml 0.2mol/L的盐酸完全反应,HCl的物质的量=0.1L×0.2mol/L=0.02mol,由AO+2HCl═ACl2+H2O,可知0.4gAO的物质的量为0.01mol,则M(AO)=0.4g0.01mol=40g/mol,故A的摩尔质量为40g/mol-16g/mol=24g/mol,A原子核内质子数目与中子数目相等,则质子数为12,即A为Mg元素;B元素原子核外电子数比A元素原子核外电子数多1,则B为Al;C-比A元素的离子多1个电子层,则C的质子数为18-1=17,即C为Cl元素;D元素原子最外层电子数是次外层电子数的2倍,原子只能有2个电子层,最外层电子数为4,即D为C元素,
(1)综上所述,A为Mg,B为Al,名称分别为镁和铝,故答案为:镁;铝;
(2)Cl的质子数为17,离子结构示意图为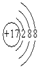 ,故答案为:
,故答案为: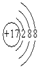 ;
;
(3)D为碳元素,最高价氧化物为CO2,分子中C原子与O原子之间形成2对共用电子对,其电子式为: ,故答案为:
,故答案为: ;
;
(4)Cl、Mg两元素形成的化合物为MgCl2,MgCl2属于离子化合物,Mg最外层两个电子被两个Cl原子得到,用电子式表示形成过程为: ,故答案为:
,故答案为: ;
;
(5)Al与氢氧化钠反应生成偏铝酸钠和氢气,离子反应方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑,故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑.
点评 本题考查位置结构性质关系及其应用,侧重对化学用语的考查,推断元素是解答关键,题目难度中等.

 阅读快车系列答案
阅读快车系列答案| A. | 电解水:2H20=2H2↑+O2↑ | B. | 4Fe(OH)2+O2+2H2O=4Fe(OH)3 | ||
| C. | 2F2+H2O=4HF+O2 | D. | 3NO2+H2O=2HNO3+NO |
| A. | 电离常数随着弱电解质浓度的增大而增大 | |
| B. | CH3COOH的电离常数表达式为Ka=c(CH3COOH)c(H+)•c(CH3COO−) | |
| C. | 电离常数只受温度影响,与浓度无关 | |
| D. | CH3COOH溶液中加入少量CH3COONa固体,电离常数减小 |
| A. | 非金属性:F>Cl>Br>I | B. | 单质氧化性:F2>Cl2>Br2>I2 | ||
| C. | 氢化物稳定性:HF>HCl>HBr>HI | D. | 沸点:F2>Cl2>Br2>I2 |
| A. | F-的结构示意图: | B. | CO2的分子模型示意图: | ||
| C. | N2的结构式::N≡N: | D. | CSO的电子式: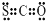 |
| A. | 聚氯乙烯一次性超薄袋可用于包装食品 | |
| B. | 利用电渗析法和离子交换法能获得纯净水 | |
| C. | 体积分数为95%的酒精用作医用酒精 | |
| D. | 石油裂化的目的是得到乙烯、丙烯等化工原料 |
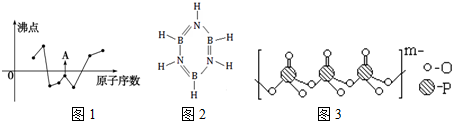


 (苯胺,弱碱性,易氧化)
(苯胺,弱碱性,易氧化)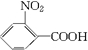 .
. .
.