题目内容
【题目】用如图所示装置进行实验(a、b电极均为Ag单质),观察到了灵敏电流计指针发生偏转。下列说法正确的是
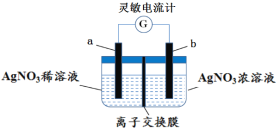
A.b极电极反应式为Ag–e–= Ag+
B.离子交换膜为阴离子交换膜
C.去掉离子交换膜,电流表仍然有电流通过
D.电流计指针不再偏转时,右边硝酸银溶液的物质的量浓度依然大于左边
【答案】B
【解析】
由于AgNO3溶液浓度不同形成浓差电池,左池为稀的AgNO3溶液,右池为浓的AgNO3溶液,Ag+浓度越大氧化性越强,所以b为正极,发生还原反应,电极反应式为Ag++e-=Ag;a为负极,发生氧化反应,电极反应式为Ag-e-=Ag+,因正极与负极消耗或生成的Ag+相等,但负极Ag减少、正极Ag增加,溶液中迁移的离子不可能是Ag+,只能是NO3-穿过交换膜向负极移动,据此解答。据此解答。
A.浓差电池中,右池AgNO3溶液浓度高,Ag+浓度越大氧化性越强,所以b为正极,电极反应式为Ag++e-=Ag,A错误;
B.负极Ag减少、正极Ag增加,左侧溶液中Ag+增大,右侧溶液中由于Ag+放电而导致附近溶液中NO3-增大,为了维持电荷平衡,溶液中NO3-穿过交换膜由右侧向左侧的负极a区移动,因此离子交换膜为阴离子交换膜,B正确;
C.若去掉离子交换膜,溶液中离子扩散,最终形成均一浓度的溶液,没有浓度差,且两个电极材料相同,不能构成原电池,故电流表不会有电流通过,C错误;
D.随着反应进行,左右两池浓度的差值逐渐减小,NO3-穿过交换膜向负极移动的速率将减小,外电路中电流将减小,电流计指针偏转幅度逐步变小,当左右两侧离子浓度相等时,电池将停止工作、不再有电流产生,此时溶液中左、右边硝酸银溶液的物质的量浓度相等,D错误;
故合理选项是B。

练习册系列答案
相关题目