题目内容
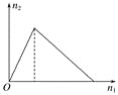
【题目】将物质X逐渐加入Y溶液中,生成沉淀的物质的量n2与所加X的物质的量n1的关系如图所示,符合如图所示的情况是( )
A.X为氢氧化钠,Y为氯化铝
B.X为氯化铝,Y为氢氧化钠
C.X为盐酸,Y为偏铝酸钠
D.X为偏铝酸钠,Y为盐酸
【答案】C
【解析】
由图可知,将物质X逐渐加入Y溶液中,生成沉淀,当Y溶液反应完后,继续加入物质X,物质X能与沉淀反应而使生成的沉淀溶解,且生成沉淀所需要的X的物质的量与沉淀溶解需要的X的物质的量之比为1:3,据此解答。
A.氢氧化钠溶液中滴入氯化铝溶液,先发生反应Al3++3OH-=Al(OH)3↓,生成Al(OH)3沉淀,当氯化铝溶液反应完后,再滴入氢氧化钠溶液发生反应Al(OH)3+OH-=AlO2-+2H2O,沉淀溶解至最后消失,所以前后两个过程氢氧化钠的物质的量之比为3:1,不符合图中所示情况,A错误;
B.氯化铝溶液中加入氢氧化钠溶液中,先发生反应Al3++4OH-=AlO2-↓+2H2O,不生成沉淀,当氢氧化钠溶液反应完后,再滴入氯化铝溶液发生反应后发生3AlO2-+Al3++6H2O=4Al(OH)3↓+6H2O,生成沉淀,与图象不符合,B错误;
C.盐酸加入偏铝酸钠溶液中,先发生反应AlO2-+H++H2O=Al(OH)3↓,生成Al(OH)3沉淀,当偏铝酸钠溶液反应完后,再继续加入盐酸发生反应Al(OH)3+3H+=Al3++3H2O,沉淀消失,所以前后两个过程HCl的物质的量之比为1:3,符合图中所示情况,C正确;
D.偏铝酸钠溶液加入盐酸中,先发生反应AlO2-+4H+=Al3++2H2O,开始不生成沉淀,当盐酸溶液反应完后,再滴入偏铝酸钠溶液3AlO2-+Al3++6H2O=4Al(OH)3↓+6H2O,生成沉淀直到最大,不符合图中所示情况,D错误;
故合理选项是C。

 互动英语系列答案
互动英语系列答案