题目内容
下列关于强弱电解质的叙述正确的是( )
| A、KCl溶液在电流作用下电离成K+和Cl- |
| B、SO2溶于水能部分转化成离子,故SO2属于弱电解质 |
| C、CaSO4微溶于水,所以CaSO4属弱电解质 |
| D、同一弱电解质的溶液,当温度、浓度不同时,其导电能力也不相同 |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:A.电离无需通电;
B.硫酸氢钠是盐,也能电离出氢离子;
C.液态氯化氢只有氯化氢分子;
D.根据电解质的概念进行解答.
B.硫酸氢钠是盐,也能电离出氢离子;
C.液态氯化氢只有氯化氢分子;
D.根据电解质的概念进行解答.
解答:
解:A.KCl溶液在水分子的作用下电离出K+和Cl-,无需通电,故A错误;
B.SO2溶于水生成亚硫酸电离出部分离子,不是SO2自身电离,所以属于非电解质,故B错误;
C.CaSO4微溶于水,但溶解的完全电离,所以CaSO4属强电解质,故C错误;
D.同一弱电解质的溶液,当温度、浓度不同时,溶液中自由移动的离子浓度不同,其导电能力也不相同,故D正确;
故选D.
B.SO2溶于水生成亚硫酸电离出部分离子,不是SO2自身电离,所以属于非电解质,故B错误;
C.CaSO4微溶于水,但溶解的完全电离,所以CaSO4属强电解质,故C错误;
D.同一弱电解质的溶液,当温度、浓度不同时,溶液中自由移动的离子浓度不同,其导电能力也不相同,故D正确;
故选D.
点评:本题主要考查电解质的概念,注意电解质和非电解质都必须是化合物,电解质能导电是溶于水溶液中或在熔融状态下自身电离,题目较简单.

练习册系列答案
相关题目
下列说法正确的是( )
| A、1H、2H、3H互为同位素 |
| B、O2、O3互为同位素 |
C、氮分子的电子式 |
| D、酸性:H2SO4>HClO4 |
下列叙述错误的是( )
(1)若R的含氧酸的酸性大于Q的含氧酸的酸性,则非金属性R强于Q
(2)阴、阳离子通过静电吸引形成的化学键叫离子键
(3)都是由非金属元素形成的化合物只能是共价化合物.
(1)若R的含氧酸的酸性大于Q的含氧酸的酸性,则非金属性R强于Q
(2)阴、阳离子通过静电吸引形成的化学键叫离子键
(3)都是由非金属元素形成的化合物只能是共价化合物.
| A、全部 | B、(1) |
| C、(2) | D、(3) |
化学与生产、生活、社会密切相关.下列有关说法中不正确的是( )
| A、新能源汽车的推广与使用有助于减少光化学烟雾的产生 |
| B、针对甲型H1N1流感的扩散情况,要加强对环境、个人的消毒预防.其中消毒剂常选用含氯消毒剂、酒精、双氧水等适宜的物质 |
| C、华裔科学家高琨在光纤传输信息领域中取得突破性成就,光纤的主要成分是高纯度的单质硅 |
| D、建国60周年庆典晚会上,天安门广场燃放的焰火是某些金属元素魅力的展现 |
下列化学式中只能表示一种物质的是( )
| A、C3H7OH |
| B、CH2O2 |
| C、C4H6 |
| D、C3H6O2 |
下列实验设计和结论正确的是( )
| A、采用加热蒸干高锰酸钾溶液的方法获得高锰酸钾晶体 |
| B、过滤时,为了加快过滤速率,可用玻璃棒在漏斗内搅拌 |
| C、某气体能使湿润的红色石蕊试纸变蓝,该气体水溶液一定显碱性 |
| D、某无色溶液中加Ba(NO3)2溶液,再加入稀盐酸,沉淀不溶解,则原溶液中一定有SO42- |
下列叙述正确的是( )
A、S2-的结构示意图是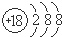 |
B、HCl的电子式为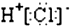 |
C、NH3的结构式为  |
| D、还原性:HCl>H2S |
用FeCl3溶液腐蚀印刷电路板上铜箔的反应是:2Fe3++Cu=2Fe2++Cu2+,该反应的还原剂是( )
| A、Fe3+ |
| B、Cu |
| C、Fe2+ |
| D、Cu2+ |
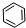 、④HCHO其中碳原子采取sp2杂化的分子有
、④HCHO其中碳原子采取sp2杂化的分子有