题目内容
标准状况下,0.1mol分子式为CmHn的有机化合物在氧气中完全燃烧,将产物依次通入浓硫酸和澄清石灰水,测得浓硫酸增重9.0g,沉淀的物质的量为0.4mol.试计算:
(1)该有机化合物的分子式;
(2)写出其可能的结构简式并命名;
(3)计算该物质燃烧消耗标准状况下氧气的体积.
(1)该有机化合物的分子式;
(2)写出其可能的结构简式并命名;
(3)计算该物质燃烧消耗标准状况下氧气的体积.
考点:有关有机物分子式确定的计算
专题:烃及其衍生物的燃烧规律
分析:浓硫酸增重9g为燃烧生成水的质量,沉淀0.4mol为碳酸钙的物质的量,根据原子守恒计算烃的分子式,结合分子式书写烃可能的结构,根据1mol烃CxHy的耗氧量为(x+
)mol,据此计算消耗氧气的物质的量,再根据V=nVm计算消耗氧气的体积.
| y |
| 4 |
解答:
解:(1)浓硫酸增重9g为燃烧生成水的质量,其物质的量=
=0.5mol,沉淀0.4mol为碳酸钙的物质的量,根据H原子守恒,烃分子中H原子数目=
=10,根据C原子守恒,烃分子中C原子数目=
=4,故该烃的分子式为:C4H10,
答:该烃的分子式为C4H10;
(2)烃的分子式为C4H10,属于烷烃,可能的结构有:CH3CH2CH2CH3、CH(CH3)3,
答:该烃可能结构简式有:CH3CH2CH2CH3、CH(CH3)3;
(3)0.1molC4H10,完全燃烧,消耗氧气的物质的量=0.1mol×(4+
)=0.65mol,标况下消耗氧气的体积为0.65mol×22.4L/mol=14.56L,
答:该物质燃烧消耗标准状况下氧气的体积为14.56L.
| 9g |
| 18g/mol |
| 0.5mol×2 |
| 0.1mol |
| 0.4mol |
| 0.1mol |
答:该烃的分子式为C4H10;
(2)烃的分子式为C4H10,属于烷烃,可能的结构有:CH3CH2CH2CH3、CH(CH3)3,
答:该烃可能结构简式有:CH3CH2CH2CH3、CH(CH3)3;
(3)0.1molC4H10,完全燃烧,消耗氧气的物质的量=0.1mol×(4+
| 10 |
| 4 |
答:该物质燃烧消耗标准状况下氧气的体积为14.56L.
点评:本题考查有机物分子式确定、同分异构体书写、有机物燃烧计算等,难度不大,注意理解掌握燃烧法利用原子守恒确定有机物的组成.

练习册系列答案
相关题目
 往一体积不变的密闭容器中充入H2(g)+I2(g)?2HI(g);△H<0,当达到平衡后,t1时,若保持混合气体总物质的量不变而改变某一反应条件,使容器内压强增大(如图所示),下列说法正确的是( )
往一体积不变的密闭容器中充入H2(g)+I2(g)?2HI(g);△H<0,当达到平衡后,t1时,若保持混合气体总物质的量不变而改变某一反应条件,使容器内压强增大(如图所示),下列说法正确的是( )| A、t1时,减小体积或升高体系温度 |
| B、平衡不移动,混合气体的密度增大 |
| C、H2的转化率增大,HI的平衡浓度减小 |
| D、容器内气体颜色变深,平均相对分子质量不变 |
 实验室需要0.80mol?L-1 NaOH溶液475mL和0.40mol?L-1硫酸500mL.根据这两种溶液的配制情况回答下列问题:
实验室需要0.80mol?L-1 NaOH溶液475mL和0.40mol?L-1硫酸500mL.根据这两种溶液的配制情况回答下列问题: 实验室需用230mL 0.1mol/L的Na2CO3溶液,填空并回答下列问题:
实验室需用230mL 0.1mol/L的Na2CO3溶液,填空并回答下列问题: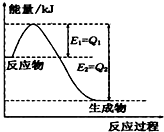 (1)一定条件下,N2和H2反应生成lmolNH3过程中能量变化如右图所示,则1mol N2完全反应时的焓变为:
(1)一定条件下,N2和H2反应生成lmolNH3过程中能量变化如右图所示,则1mol N2完全反应时的焓变为:
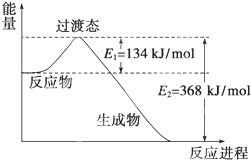 (1)如图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:
(1)如图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式: