题目内容
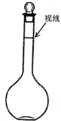 实验室需用230mL 0.1mol/L的Na2CO3溶液,填空并回答下列问题:
实验室需用230mL 0.1mol/L的Na2CO3溶液,填空并回答下列问题:(1)根据实际:应配制0.1mol/L的Na2CO3溶液
(2)在下面的操作步骤中,完成欠缺的内容:
①称取:用天平称取所需质量的Na2CO3固体.
②溶解:将称好的Na2CO3固体倒入烧杯中,再加入少量蒸馏水(约30mL),用玻璃棒慢慢搅动,使其溶解充分.
③转移:将已冷却的Na2CO3溶液
④洗涤:用30mL水洗涤烧杯2-3次,洗涤液均注入容量瓶,振荡.
⑤定容:继续往容量瓶内小心加水,直到液面接近刻度1~2cm处,
⑥摇匀:将容量瓶盖紧,振荡,摇匀.
(3)下列有关容量瓶及其使用,说法正确的有
A、容量瓶上注有容积及使用温度,并必须在其指定的情况下使用
B、使用容量瓶前检查它是否漏水
C、容量瓶用蒸馏水洗净后,先用对应的标准溶液润洗,再用来配制溶液
D、容量瓶可用来量取一定体积的溶液,也可用来长时间储存配好的溶液
(4)下列五项操作中会导致所得溶液浓度偏高的有
A.没有洗涤烧杯和玻璃棒
B.在转移过程中有溶液撒在外面
C.未冷却到室温就将溶液转移到容量瓶并定容
D.定容时观察液面的情况如右图所示(视线偏高)
E.定容后,把容量瓶反复摇匀后发现液面低于刻度线,不做任何补救措施.
考点:配制一定物质的量浓度的溶液
专题:实验题
分析:(1)容量瓶的选择规则为“大而近”,依据n=C×V、m=n×M计算碳酸钠的质量;
(2)③容量瓶瓶颈非常细,移液时应用玻璃棒引流;
⑤定容时,开始用玻璃棒引流蒸馏水如容量瓶,但是离刻度线较近时,应该有胶头滴管逐滴滴加防止加入的蒸馏水过多,加入蒸馏水的量为使溶液凹面恰好与刻度相切;
(3)容量瓶上标有温度、容量、刻度线,容量瓶使用前必须检漏;容量瓶用来配置一定物质的量浓度的溶液,使用前要先检查容量瓶是否漏液,不能用来加热,不能用容量瓶贮存配制好的溶液;
(4)依据C=
分析误差,凡是使n减小或者使V增大的操作都会使溶液的浓度偏小,反之,使溶液浓度偏大.
(2)③容量瓶瓶颈非常细,移液时应用玻璃棒引流;
⑤定容时,开始用玻璃棒引流蒸馏水如容量瓶,但是离刻度线较近时,应该有胶头滴管逐滴滴加防止加入的蒸馏水过多,加入蒸馏水的量为使溶液凹面恰好与刻度相切;
(3)容量瓶上标有温度、容量、刻度线,容量瓶使用前必须检漏;容量瓶用来配置一定物质的量浓度的溶液,使用前要先检查容量瓶是否漏液,不能用来加热,不能用容量瓶贮存配制好的溶液;
(4)依据C=
| n |
| V |
解答:
解:(1)容量瓶的选择规则为“大而近”,要配230ml的溶液,应选择250ml的容量瓶;
应称Na2CO3固体的物质的量n=C×V=0.1mol/L×0.25L=0.025mol,其质量m=n×M=0.025mol×106g/mol≈2.7g;
故答案为:250;2.7;
(2)容量瓶瓶颈非常细,移液时应用玻璃棒引流;
定容时,开始用玻璃棒引流蒸馏水如容量瓶,但是离刻度线较近时,应该有胶头滴管逐滴滴加防止加入的蒸馏水过多,加入蒸馏水的量为使溶液凹面恰好与刻度相切;
故答案为:③沿玻璃棒注入固定容量的容量瓶中;
⑤改用胶头滴管加水,使溶液凹面恰好与刻度相切;
(3)A、容量瓶上注有容积及使用温度,并必须在其指定的情况下使用,故A正确;
B、使用容量瓶前检查它是否漏水,故B正确;
C、容量瓶用蒸馏水洗净后,先用对应的标准溶液润洗,再用来配制溶液,导致所配溶液浓度偏高,故C错误;
D、容量瓶为精密仪器,不能用来长时间储存配好的溶液,故D错误;
故选:AB;
(4)依据C=
分析误差,凡是使n减小或者使V增大的操作都会使溶液的浓度偏小,反之,使溶液浓度偏大.
A.没有洗涤烧杯和玻璃棒,溶质的物质的量n减小,所配溶液浓度偏小,故A不选;
B.在转移过程中有溶液撒在外面,溶质的物质的量n减小,所配溶液浓度偏小,故B不选;
C.未冷却到室温就将溶液转移到容量瓶并定容,冷却到室温后,溶液的体积V偏小,所配溶液的浓度偏大,故C选;
D.定容时观察液面的情况如右图所示(视线偏高),导致加入的蒸馏水偏少,溶液的体积V偏小,所配溶液的浓度偏大,故D选;
E.定容后,把容量瓶反复摇匀后发现液面低于刻度线,是因为部分溶液沾到瓶塞和瓶壁上,属于正常操作,对溶液浓度无影响,不做任何补救措施,故E不选;
故选:CD.
应称Na2CO3固体的物质的量n=C×V=0.1mol/L×0.25L=0.025mol,其质量m=n×M=0.025mol×106g/mol≈2.7g;
故答案为:250;2.7;
(2)容量瓶瓶颈非常细,移液时应用玻璃棒引流;
定容时,开始用玻璃棒引流蒸馏水如容量瓶,但是离刻度线较近时,应该有胶头滴管逐滴滴加防止加入的蒸馏水过多,加入蒸馏水的量为使溶液凹面恰好与刻度相切;
故答案为:③沿玻璃棒注入固定容量的容量瓶中;
⑤改用胶头滴管加水,使溶液凹面恰好与刻度相切;
(3)A、容量瓶上注有容积及使用温度,并必须在其指定的情况下使用,故A正确;
B、使用容量瓶前检查它是否漏水,故B正确;
C、容量瓶用蒸馏水洗净后,先用对应的标准溶液润洗,再用来配制溶液,导致所配溶液浓度偏高,故C错误;
D、容量瓶为精密仪器,不能用来长时间储存配好的溶液,故D错误;
故选:AB;
(4)依据C=
| n |
| V |
A.没有洗涤烧杯和玻璃棒,溶质的物质的量n减小,所配溶液浓度偏小,故A不选;
B.在转移过程中有溶液撒在外面,溶质的物质的量n减小,所配溶液浓度偏小,故B不选;
C.未冷却到室温就将溶液转移到容量瓶并定容,冷却到室温后,溶液的体积V偏小,所配溶液的浓度偏大,故C选;
D.定容时观察液面的情况如右图所示(视线偏高),导致加入的蒸馏水偏少,溶液的体积V偏小,所配溶液的浓度偏大,故D选;
E.定容后,把容量瓶反复摇匀后发现液面低于刻度线,是因为部分溶液沾到瓶塞和瓶壁上,属于正常操作,对溶液浓度无影响,不做任何补救措施,故E不选;
故选:CD.
点评:本题考查了一定物质的量浓度溶液的配置,熟悉步骤和配置原理是解题关键,注意误差分析的方法,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
某澄清透明溶液中可能含有:NH4+、Ba2+、Al3+、Fe2+、SO32-、SO42-、HCO3-中的几种离子.为确定溶液组成,进行如下实验:
①测定溶液的pH,溶液显强酸性.滴加Ba(NO3)2(aq)出现白色沉淀.
②取少量溶液加入NaOH(aq)至强碱性,产生刺激性气味的气体并得到澄清溶液.
③在②的澄清溶液中通入足量CO2,有白色沉淀生成.
由此,正确的推测是( )
①测定溶液的pH,溶液显强酸性.滴加Ba(NO3)2(aq)出现白色沉淀.
②取少量溶液加入NaOH(aq)至强碱性,产生刺激性气味的气体并得到澄清溶液.
③在②的澄清溶液中通入足量CO2,有白色沉淀生成.
由此,正确的推测是( )
| A、一定有Al3+离子 |
| B、可能有HCO3-离子 |
| C、不能确定SO32-离子是否存在 |
| D、不存在Fe2+离子,可能存在Ba2+离子 |
