题目内容
12.铅蓄电池是典型的可充型电池,它的正负极格板是惰性材料,电池总反应式为:Pb+PbO2+4H++2SO42-$?_{充电}^{放电}$2PbSO4+2H2O 请回答下列问题:已知硫酸铅不溶于水,放电时,该电池的负极反应为 Pb-2e-+SO42-=PbSO4,则正极的电极反应式是PbO2+2e-+4H++SO42-═PbSO4+2H2O;电解液中H2SO4的浓度将变小;当外电路通过1mol电子时,理论上负极板的质量增加48g.分析 根据电池反应式知,负极电解反应:Pb-2e-+SO42-=PbSO4 ,正极电极反应:PbO2+2e-+4H++2SO42-=PbSO4+2H2O,根据电池反应式确定溶液中硫酸浓度变化;根据负极上增加质量与转移电子之间的关系式计算负极板增加的质量.
解答 解:负极电解反应:Pb-2e-+SO42-=PbSO4 ,正极电极反应:PbO2+2e-+4H++2SO42-=PbSO4+2H2O,根据电池反应式知,硫酸是反应物,所以随着反应的进行,硫酸的浓度逐渐减小;
当外电路通过1mol电子时,依据电子守恒计算理论上负极板的质量增加0.5mol×303g/mol-0.5mol×207g/mol=48g;
故答案为:PbO2+2e-+4H++SO42-═PbSO4+2H2O;小;48.
点评 本题考查了原电池原理,会根据电池反应式及元素化合价变化书写正负极电极反应式,再结合各个物理量之间的关系式进行计算,注意:负极上生成难溶性的硫酸铅导致负极质量增加,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
1.X、Y、Z、W、M均为短周期主族元素,原子序数依次增加,X与W同族,X原子核外电子数与电子层数相等,Y与Z相邻,Z原子最外层电子数是其内层电子数的3倍,M在同周期中原子半径最小,则下列说法错误的是( )
| A. | X单质在M单质中燃烧产生苍白色火焰,M最高价态含氧酸是已知的最强酸 | |
| B. | Z与W可生成W2Z和W2Z2,且W2Z2溶于水时,既有离子键、极性键、非极性键的断裂,又有离子键、极性键、非极性键生成 | |
| C. | X、Y、Z三种元素形成的化合物可能含离子键、共价键 | |
| D. | X与Z可形成10电子和18电子的化合物,分子中只含极性键 |
7.乙炔分子CH≡CH加成可以得到CH2═CH-C≡CH(乙烯基乙炔),该物质是合成橡胶的重要原料.下列对该物质的判断中错误的是( )
| A. | 该物质与足量的H2加成后,只能生成一种物质 | |
| B. | 该物质既是CH2═CH2的同系物,又是CH≡CH的同系物 | |
| C. | 该物质既能使酸性KMnO4溶液褪色,又能使溴水褪色 | |
| D. | 该物质经加成,加聚后产物是氯丁橡胶( )的主要成分 )的主要成分 |
1.下面是某科学兴趣小组的同学做同周期元素性质递变规律的实验时,设计了一套实验方案.其中实验步骤如下:
请整理并完成实验报告.
(1)实验目的:探究同周期元素性质的递变规律.
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na 2S溶液,AlCl 3溶液,NaOH溶液等.
仪器:①试管,②酒精灯,③胶头滴管,试管夹,镊子,小刀,玻璃片,砂纸等.
(3)实验内容:(完成下列表格中的实验现象和化学方程式)
(4)实验结论:同周期元素随原子序数的递增,失电子能力逐渐减弱,得电子能力逐渐增强.
(5)请用原子结构的知识简单解释上述结论.
| 实验序号 | 实验步骤 |
| ① | 将镁条用砂纸打磨后,放入沸水中;再向溶液中滴加酚酞溶液 |
| ② | 向新制得的Na 2S溶液中滴加新制的氯水 |
| ③ | 将一小块金属钠放入滴有酚酞溶液的冷水中 |
| ④ | 将镁条投入稀盐酸中 |
| ⑤ | 将铝条投入稀盐酸中 |
| ⑥ | 向AlCl 3溶液中滴加NaOH溶液至过量 |
(1)实验目的:探究同周期元素性质的递变规律.
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na 2S溶液,AlCl 3溶液,NaOH溶液等.
仪器:①试管,②酒精灯,③胶头滴管,试管夹,镊子,小刀,玻璃片,砂纸等.
(3)实验内容:(完成下列表格中的实验现象和化学方程式)
| 实验序号 | 实验步骤(略) | 实验现象 | 化学方程式 |
| ① | |||
| ② | |||
| ③ | |||
| ④ | |||
| ⑤ | |||
| ⑥ |
(5)请用原子结构的知识简单解释上述结论.
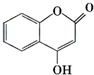 可用来制备抗凝血药,通过下列路线合成:
可用来制备抗凝血药,通过下列路线合成: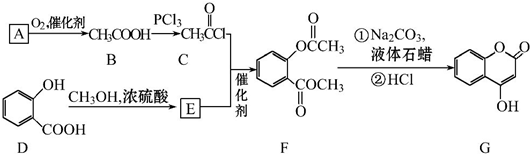
 .
. +3NaOH$\stackrel{△}{→}$
+3NaOH$\stackrel{△}{→}$ +CH3COONa+CH3OH+H2O.
+CH3COONa+CH3OH+H2O.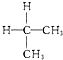 与
与 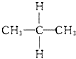
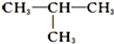
 ;
;