题目内容
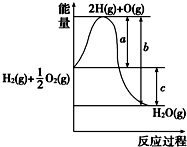
10.N2和H2合成NH3的能量变化如图所示,该反应的热化学方程式是( )
| A. | N2(g)+3H2(g)?2NH3(g);△H=2(b-a) kJ/mol | |
| B. | N2(g)+3H2(g)?2NH3(l);△H=2(a-b-c) kJ/mol | |
| C. | $\frac{1}{2}$N2(g)+$\frac{3}{2}$H2(g)?NH3(l);△H=(b+c-a) kJ/mol | |
| D. | $\frac{1}{2}$N2(g)+$\frac{3}{2}$H2(g)?NH3(g);△H=(a+b) kJ/mol |
分析 从图象看,热化学方程式为:①$\frac{1}{2}$N2(g)+$\frac{1}{2}$H2(g)?NH3(l);△H=-(b+c-a) kJ/mol;或②$\frac{1}{2}$N2(g)+$\frac{1}{2}$H2(g)?NH3(g);△H=(a-b) kJ/mol,△H与化学计量数成正比,以此分析.
解答 解:从图象看,热化学方程式为:①$\frac{1}{2}$N2(g)+$\frac{1}{2}$H2(g)?NH3(l);△H=-(b+c-a) kJ/mol或②$\frac{1}{2}$N2(g)+$\frac{1}{2}$H2(g)?NH3(g);△H=(a-b) kJ/mol;△H=(a-b) kJ/mol,△H与化学计量数成正比,①×2可得:N2(g)+3H2(g)═2NH3(l)△H=2(a-b-c) kJ/mol,
②×2可得:N2(g)+3H2(g)═2NH3(g)△H=2(a-b) kJ/mol,
故选B.
点评 本题考查热化学方程式的书写,题目难度不大,侧重于数据分析和转化能力的培养,注意书写热化学方程式的注意事项以及反应热的计算方法.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
20.第十届亲水胶体国际会议于2010年6月20日到24日在上海举行,专家学者共同研讨亲水胶体和应用领域中关注的问题,下列说法错误的是( )
| A. | 利用丁达尔效应可区分溶液与胶体 | |
| B. | 胶体区别于其它分散系的本质特征是分散质的微粒直径在10-9~10-7m之间 | |
| C. | 胶体分散质粒子能透过半透膜和滤纸 | |
| D. | Fe(OH)3胶体吸附水中的悬浮颗粒并沉降,达到净水的目的 |
5.将5.6g的Zn-Cu混合物完全溶解于足量的硝酸中,收集反应产生的x气体.再向所得溶液中加入适量的NaOH溶液,产生15.8g沉淀.根据题意推断气体x的成分可能是( )
| A. | 0.3molNO2和0.3molNO | |
| B. | 0.1mol NO、0.2molNO2和0.05mol N2O4 | |
| C. | 0.2molNO2 和0.1molN2O4 | |
| D. | 0.6molNO |
15.下列推断正确的是( )
| A. | SiO2是酸性氧化物,能与NaOH溶液反应 | |
| B. | Na2O、Na2O2组成元素相同,与CO2反应产物也相同 | |
| C. | CO、CO2都是大气污染气体,在空气中都能稳定存在 | |
| D. | 新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色 |
2.下列说法不正确的是( )
| A. | 液氯可以装入钢瓶中贮存 | |
| B. | 氯水可漂洗衣服上的墨渍 | |
| C. | 实验室使用的氯水要装在棕色瓶中,并且随配随用 | |
| D. | 实验室可利用强氧化剂如KMnO4、KClO3等与浓HCl反应的原理制Cl2 |


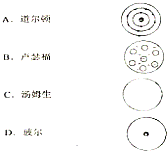 (1)将下列科学家与他们的原子结构模型(如图)用线连接起来:
(1)将下列科学家与他们的原子结构模型(如图)用线连接起来: