题目内容
14.以锌片和铜片为电极,以稀硫酸为电解质溶液的原电池中,当导线中通过2mol电子时,下列说法正确的是( )| A. | 锌片溶解了1mol,铜片上析出1mol氢气 | |
| B. | 锌片发生还原反应 | |
| C. | 正极附近的SO42-离子浓度逐渐增大 | |
| D. | 电池工作时,电子由正极通过外电路流向负极 |
分析 锌片、铜片和稀硫酸构成原电池,较活泼的金属Zn作负极,铜作正极,负极反应为Zn-2e-=Zn2+,发生氧化反应;正极上氢离子得电子发生氢气,发生还原反应,以此来解答.
解答 解:A.负极反应为Zn-2e-=Zn2+,正极反应为2H++2e-=H2↑,转移2mol电子溶解1molZn,且生成1molH2,故A正确;
B.Zn作负极,发生氧化反应,故B错误;
C.阴离子向负极移动,故负极附近SO42-离子浓度逐渐增大,故C错误;
D.电子由负极通过外电路流向正极,故D错误;
故选A.
点评 本题考查了原电池原理,把握发生的电极反应、电池总反应及物质的量的关系为解答本题的关键,侧重原电池工作原理的考查,题目难度不大.

练习册系列答案
相关题目
5.面粉厂严禁烟火的主要原因( )
| A. | 防止火灾发生 | B. | 防止污染面粉 | ||
| C. | 吸烟有害健康 | D. | 面粉颗粒极易被引燃而发生爆炸 |
2.下列说法不正确的是( )
| A. | 石油的分馏可以得到烷烃、环烷烃、芳香烃等产品 | |
| B. | 将石油裂化、裂解,综合利用石油资源 | |
| C. | 有节制地开采煤、石油、天然气等矿物资源 | |
| D. | 用于奥运火炬的丙烷是一种清洁燃料 |
9.下列说法可以证明反应N2+3H2?2NH3已达到平衡状态的是( )
| A. | 消耗1mol N2的同时,生成2mol NH3 | |
| B. | N2、H2、NH3的反应速率比为1:3:2的状态 | |
| C. | 1mol N≡N键断裂的同时,有6mol N-H 键断裂 | |
| D. | N2和H2浓度相等的时候 |
19.下列化合物的结构中,只含有离子键的是( )
| A. | H2O | B. | NaCl | C. | NaOH | D. | CO2 |

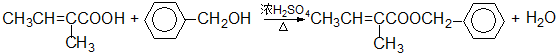


 +
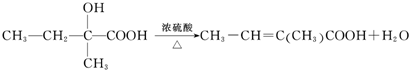
+ $\stackrel{△}{→}$
$\stackrel{△}{→}$
 .
. .
. 和
和 结构的D的所有同分异构共有9种(含顺反异构体),写出其中任意一种含反式结构的结构简式
结构的D的所有同分异构共有9种(含顺反异构体),写出其中任意一种含反式结构的结构简式 .
. 用系统命名法命名该烃:2,3-二甲基戊烷.
用系统命名法命名该烃:2,3-二甲基戊烷.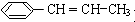 )在催化剂作用下生成聚苯丙烯的反应方程式:
)在催化剂作用下生成聚苯丙烯的反应方程式: .
. .
.